题目内容
【题目】(1)过氧化钠保存不当容易变质,生成Na2CO3。判断过氧化钠在空气中是否变质的简单方法是观察颜色是否 。
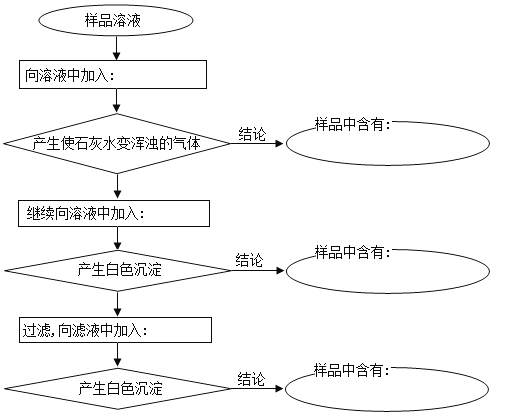
(2)某过氧化钠样品已经部分变质,可以取少量样品,溶解,加入 溶液,充分振荡,看是否有白色沉淀,通过判断溶液中含有碳酸根来证明Na2O2已经变质
(3)检验样品中还有过氧化钠的方法是:取少量样品放入试管中,再加入适量的水,用 ,通过验证反应产生了氧气来证明样品中仍有Na2O2
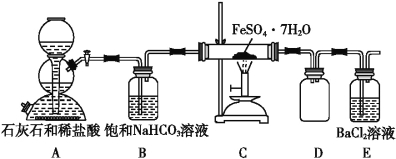
(4)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。

上图中的E和F构成量气装置,用来测定O2的体积。
写出装置A中发生反应的离子方程式:
装置B的作用是除去混在二氧化碳中的氯化氢气体,
NaOH的作用是
他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
【答案】(1)由淡黄色变成白色
(2)BaCl2或CaCl2或Ca(OH)2都可以
(3)带有火星的木条伸入试管中,木条复燃
(4)①CaCO3+2H+=Ca2++H2O+CO2↑②吸收未反应的CO2③![]()
【解析】
试题分析:(1)过氧化钠呈淡黄色,保存不当容易变质,生成白色Na2CO3。判断过氧化钠在空气中是否变质的简单方法是观察颜色是否由淡黄色变成白色;(2)过氧化钠保存不当容易变质,生成白色Na2CO3,检查过氧化钠是否变质,只需检验CO32-,溶解,加入BaCl2或CaCl2溶液,充分振荡,看是否有白色碳酸钙或碳酸钡沉淀生成,证明Na2O2已经变质;(3)过氧化钠与水反应生成氧气,若样品中有过氧化钠,则加入水中有氧气生成:取少量样品放入试管中,再加入适量的水,用带有火星的木条伸入试管中,若木条复燃,则含有过氧化钠;(4)①写出装置A中碳酸钙与盐酸反应生成二氧化碳,反应的离子方程式CaCO3 + 2H+=Ca2+ +H2O +CO2↑;C出来的气体含有二氧化碳,②NaOH的作用是吸收未反应的CO2;样品中过氧化钠的质量分数为x%
![]()
156 g 22.4L
ax ![]()
![]()
X%=![]() 。
。