题目内容
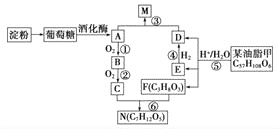
【题目】现有中学化学常见的物质,其中甲、乙、丙是单质,甲为第三周期金属,A、B、C、D、E、F是化合物,B是红棕色气体,C在常温下是无色无味液体,甲元素的原子序数是丙元素原子序数的2倍,它们之间有如图所示的相互转化关系(部分反应条件已略去).
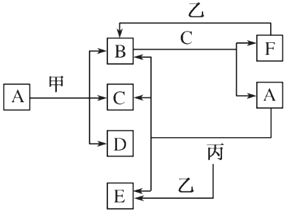
(1)B的化学式为 ,D的化学式为 .
(2)写出A与丙反应的化学方程式: .
(3)工业上制取A分三步进行,其中两步反应已经在图中得到体现,写出另外一步反应的化学方程式: .
(4)若9.6g甲与一定量A浓溶液完全反应后,生成标准状况下的8.96L气体中含有的B和F,且甲无剩余,则B和F的物质的量之比为 .
【答案】(1)NO2;Mg(NO3)2;
(2)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(3)4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(4)1:1.
【解析】
试题分析:B是红棕色气体,B是NO2;C在常温下是无色无味液体,则C为H2O,甲为第三周期金属,甲元素的原子序数是丙元素原子序数的2倍,甲的原子序数为偶数,则原子序数为12,即甲为Mg,则丙为C;结合转化可知,A溶液是浓硝酸,则D为Mg(NO3)2,B与C生成F,F为NO,F与乙生成B,则乙为O2,由丙和A的反应C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O可知,E为CO2,以此来解答.
CO2↑+4NO2↑+2H2O可知,E为CO2,以此来解答.
解:B是红棕色气体,B是NO2;C在常温下是无色无味液体,则C为H2O,甲为第三周期金属,甲元素的原子序数是丙元素原子序数的2倍,甲的原子序数为偶数,则原子序数为12,即甲为Mg,则丙为C;结合转化可知,A溶液是浓硝酸,则D为Mg(NO3)2,B与C生成F,F为NO,F与乙生成B,则乙为O2,由丙和A的反应C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O可知,E为CO2,
CO2↑+4NO2↑+2H2O可知,E为CO2,
(1)由上述分析可知,B为NO2,D为Mg(NO3)2,故答案为:NO2;Mg(NO3)2;
(2)A与丙反应的化学方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(3)制取A分三步进行,氨气的催化氧化、NO氧化生成二氧化氮、二氧化氮与水反应生成硝酸,则除图中转化外的另外一步反应的化学方程式为4NH3+5O2![]() 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(4)n(Mg)=![]() =0.4mol,8.96L气体中含有的B和F,气体的物质的量为
=0.4mol,8.96L气体中含有的B和F,气体的物质的量为![]() =0.4mol,Mg完全反应,设B和F的物质的量分别为x、y,由电子守恒及原子守恒可知,
=0.4mol,Mg完全反应,设B和F的物质的量分别为x、y,由电子守恒及原子守恒可知,![]() ,解得x=0.2mol,y=0.2mol,所以B和F的物质的量之比为1:1,故答案为:1:1.
,解得x=0.2mol,y=0.2mol,所以B和F的物质的量之比为1:1,故答案为:1:1.

【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D