题目内容
【题目】下列说法正确的是( )
A.1molN2与4mol H2混合充分反应,则反应中转移的电子数目为6mol
B.反应2Mg(s)+CO2(g)=C(s)+2MgO(s) 能自发进行,则该反应的ΔH>0
C.向0.1mol·L1 CH3COONa溶液中加入少量水,溶液中 减小
减小
D.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉就会溶解
【答案】D
【解析】
A.该反应为可逆反应,反应物不能完全转化为生成物,则反应中转移电子数无法计算,A错误;
B.该反应能自发进行,则△G=△H-T△S<0,该反应△S<0,要使该反应△G=△H-T△S<0,△H<0,B错误;
C.加水稀释促进醋酸根离子水解且溶液体积增大导致c(CH3COO-)减小,温度不变电离平衡常数不变,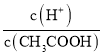 =
=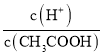 ×
×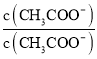 =
=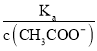 增大,C错误;
增大,C错误;
D.在稀硫酸中加入铜粉,稀硫酸不与铜反应,则铜粉不溶解;再加入Cu(NO3)2固体,硝酸根离子在酸性条件下能够氧化铜,则铜粉就会溶解,D正确;
故合理选项是D。

 小学能力测试卷系列答案
小学能力测试卷系列答案【题目】雾霾天气频繁出现,严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)汽车尾气中NOx和CO的生成:已知汽缸中生成NO的反应为:N2(g)+O2(g)![]() 2NO(g)△H>0。恒温,恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是________
2NO(g)△H>0。恒温,恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是________
A.混合气体的密度不再变化
B.容器内的压强不再变化
C.N2、O2、NO的物质的量之比为1∶1∶2
D.氧气的百分含量不再变化
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ·mol- 1
②洗涤含SO2的烟气。
写出焦炭与水蒸气反应的热化学方程式:________________________。
(3)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”之一。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质)。一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
物质 温度/℃ | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式________________;
②计算上述反应T1℃时的平衡常数K1=________;若T1<T2,则该反应的△H_______0(填“>”、“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为________。