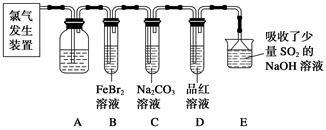
��Ŀ����
�����£���Cl2����ͨ��һ������ˮ�������ͣ�Ȼ�������ñ�����ˮ����μ���0.1mol��L-1������������Һ������������pH�仯��ͼ��ʾ�������й�������ȷ����
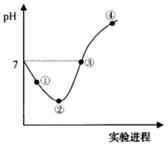

| A���ڵ�֮ǰ��������Ӧ�����ӷ���ʽΪCl2+H2O=2H++Cl��+ClO�� |
| B���۵���ʾ��Һ�У�c(Na+)= c(HClO)+2c(ClO-) |
| C��ʵ���������Һ��pH������pH��ֽ��� |
| D�����ߵ���ʼ��ˮ�ĵ���̶���� |
B
���������A���ڵ�֮ǰ������Cl2��H2O��Ӧ����HCl��HClO�ķ�Ӧ��HClOΪ���ᣬ���ܲ�����ӣ�����B���۵���Һ�����ԣ���c��H+��=c��OH-�������ݵ���غ��c��H+��+c��Na+��=c��Cl-��+c��Cl0-��+c��OH-��������c��Na+��=c��Cl-��+c��ClO-�������������غ��c��Cl-��=c��ClO-��+c��HClO��������c��Na+��=c��HClO��+2c��ClO-������ȷ��C����Ϊ��ˮ�к���HClO������Ư���ԣ�����ʵ���������Һ��pH������pH��ֽ��ã�����D��Cl2��NaOHǡ�÷�Ӧʱˮ�ĵ���̶������2�����ʡ�ͼ��ķ�����pH��ֽ��ʹ�á�����Ũ�ȱȽϡ�ˮ�ĵ��롣

��ϰ��ϵ�д�
 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
�����Ŀ