题目内容
【题目】【选修3:物质结构与性质】X、Y、M、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)基态Y原子的价电子排布图是___________;Z所在周期中第一电离能最大的主族元素是___________(元素名称)。
(2)XY2离子的立体构型是___________;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是___________(元素符号)。
(3)已知XH3易与R2+形成配离子,但XM3不易与R2+形成配离子,其原因是______________________。
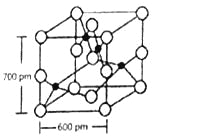
(4)Y与R所形成的化合物晶体晶胞如下图所示,该晶体的化学式:___________;晶胞参数如下图所示,则该晶胞密度是___________g·cm-3(列式并计算结果,保留小数点儿后一位)。
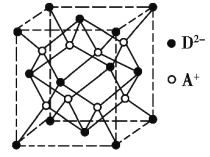
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________(填标号)。

a.CF4b.CH4c.NH4+d.H2O
【答案】(1) 氯(1分)
氯(1分)
(2)V形 O
(3)N、F、H三祌元素的电负性,F > N > H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子
(4)CuO 2.1 (5)C
【解析】试题分析:(1)X、Y、M、Z、R为前四周期元素,且原子序数依次增大,XY2是红棕色气体,则X的N元素;Y是O元素,XY2是NO2;X与氢元素可形成XH3;M是周期表中电负性最大的元素,则M是F元素;Z基态原子的M层是K层电子数的3倍,Z是S元素;R2+离子的3d轨道中有9个电子,则R是Cu元素;(1)基态Y原子的价电子排布图是![]() ;Z是S元素,同一周期的元素,原子序数越大,元素的第一电离能就越大,所以第三周期的元素中第一电离能最大的主族元素是氯元素;(2)NO2-的中心原子N原子含有的孤对电子数是:
;Z是S元素,同一周期的元素,原子序数越大,元素的第一电离能就越大,所以第三周期的元素中第一电离能最大的主族元素是氯元素;(2)NO2-的中心原子N原子含有的孤对电子数是:![]() ,即N原子的价层电子对数是3,电子含有一对孤对电子,因此其离子的立体构型是V形;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是O原子;(3)由于在N、F、H三种元素的电负性:F>N>H,所以在NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,所以XH3易与R2+形成配离子,但XM3不易与R2+形成配离子;(4)根据晶胞结构、均摊法可知,在晶胞中含有Cu原子数是8×1/8+2×1/2+4×1/4+1=4,O原子数是4×1=4,因此二者之比为4∶4 = 1∶1,化学式为CuO;该晶体的晶胞是长方体,边长分别是600pm、600pm、700pm,则该晶体的密度是
,即N原子的价层电子对数是3,电子含有一对孤对电子,因此其离子的立体构型是V形;R2+的水合离子[R(H2O)4]2+中,提供孤电子对的原子是O原子;(3)由于在N、F、H三种元素的电负性:F>N>H,所以在NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,所以XH3易与R2+形成配离子,但XM3不易与R2+形成配离子;(4)根据晶胞结构、均摊法可知,在晶胞中含有Cu原子数是8×1/8+2×1/2+4×1/4+1=4,O原子数是4×1=4,因此二者之比为4∶4 = 1∶1,化学式为CuO;该晶体的晶胞是长方体,边长分别是600pm、600pm、700pm,则该晶体的密度是 ;(5)在该分子中的四个N原子构成的是正四面体结构,若再分子内的空腔中能嵌入某离子或分子并形成4个氢键予以识别,则应该是含氢化物或离子,其微粒结构也应该是正四面体结构,在选项中的微粒中只有NH4+是正四面体结构,四个氢原子位于正四面体的四个顶点上,答案选C。
;(5)在该分子中的四个N原子构成的是正四面体结构,若再分子内的空腔中能嵌入某离子或分子并形成4个氢键予以识别,则应该是含氢化物或离子,其微粒结构也应该是正四面体结构,在选项中的微粒中只有NH4+是正四面体结构,四个氢原子位于正四面体的四个顶点上,答案选C。