题目内容
8.质量比为11:7:6的CO2、CO、NO,其物质的量之比为5:5:4,它们所含分子数之比为5:5:4,所含氧原子数之比为5:2:2.分析 根据公式m=nM=$\frac{N}{{N}_{A}}$M来进行计算即可.
解答 解:质量比为11:7:6的CO2、CO、NO,其物质的量之比为$\frac{11}{44}$:$\frac{7}{28}$:$\frac{6}{30}$=5:5:4,它们所含分子数之比等于物质的量之比,即为5:5:4,所含的氧原子数之比是(5:2):4:4=5:2:2,
故答案为:5:4:4;5:4:4;5:2:2.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意相关计算公式的运用,把握物质的构成特点,难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
18.下列物质类属、名称(或俗名)及化学式相符的是( )
| A. | 碱性氧化物 氧化亚铁 Fe2O3 | B. | 酸性氧化物 干冰 CO2 | ||
| C. | 酸 硫酸 H2SO3 | D. | 碱 纯碱 Na2CO3 |
19.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,18g H2O的体积是22.4L | |
| B. | 在常温、常压下,11.2L N2含有的分子数为0.5NA | |
| C. | 标准状况下,22.4LNH3所含的分子数目为NA | |
| D. | 1 mo1•L-1 NaCl溶液中所含有的Na+离子数目为NA |
16.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1mol/L的Ca(ClO)2溶液中含ClO-数目为2NA | |
| B. | 标准状况下,22.4L三氯甲烷的原子数约为4 NA个 | |
| C. | 体积分别为1.0L pH═2的盐酸与硫酸溶液中氢离子数均为0.01NA | |
| D. | 1mol-OH与1 molOH-所含电子数均为9NA |
3.CO2的资源化利用是解决温室效应的重要途径,在一定条件下利用NH3 捕获CO2 生成重要化工产品三聚氰酸(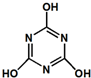 )下列关于三聚氰酸的说法正确( )
)下列关于三聚氰酸的说法正确( )
 )下列关于三聚氰酸的说法正确( )
)下列关于三聚氰酸的说法正确( )| A. | 三聚氰酸属于单质 | B. | 三聚氰酸属于氧化物 | ||
| C. | 三聚氰酸属于有机化合物 | D. | 三聚氰酸属于混合物 |
13.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4L四氯化碳CCl4含有的分子数为NA | |
| B. | 常温常压下,18g水含有的分子数为 NA | |
| C. | 1molCu和足量浓硝酸反应产生NO分子数为NA | |
| D. | 1.0mol•L-1 Na2CO3溶液中含有CO32-数为 NA |
17.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是( )
| A. | NH4+、Cu2+、Cl-、NO3- | B. | K+、Na+、SO32-、S2- | ||
| C. | K+、Na+、CO32-、SO42- | D. | Ba2+、Na+、HCO3-、Br- |
18.含有一个碳碳双键的烯烃,与H2加成后结构简式为: ,此烯烃的结构简式有( )
,此烯烃的结构简式有( )
 ,此烯烃的结构简式有( )
,此烯烃的结构简式有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |