题目内容
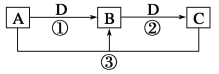
【题目】常见无机物A、B、C、D存在如图转化关系:
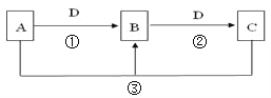
(1)若D是氯碱工业的主要产品,B有两性氢氧化物,则反应②的离子方程式是: 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
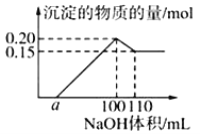
(3)若A为常见挥发性强酸,D是生产生活中用量最大用途最广的金属单质,,则B的化学式可能是 ,写出反应②的离子方程式为 。
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式 。
(5)若A、B、C的水溶液均显碱性,焰色反应均为黄色,D为CO2,用离子方程式解释B溶液显碱性的原因(用离子方程式表示)___________,举出C的一种用途_______。
【答案】(1)Al(OH)3+OH—=[Al(OH)4]—
(2)4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
(3)Fe(NO3)3 ;2Fe3+ +Fe=3Fe2+(4)2H2S+SO2=3S+2H2O
(5)CO32-+H2O![]() HCO3-+OH- 治疗胃酸过多、发酵粉、泡沫灭火器等
HCO3-+OH- 治疗胃酸过多、发酵粉、泡沫灭火器等
【解析】
试题分析:(1)若D是氯碱工业的主要产品,B有两性氢氧化物,则B是氢氧化铝,D是氢氧化钠,A是铝盐,C是偏铝酸盐,因此反应②的离子方程式是Al(OH)3+OH—=[Al(OH)4 ]—。
(2)若A是一种碱性气体,常用作制冷剂,A是氨气,B是汽车尾气之一,遇空气会变色,B是NO,所以D是氧气,C是NO2,所以反应①的化学方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。
(3)若A为常见挥发性强酸,因此A是硝酸,D是生产生活中用量最大用途最广的金属单质,则D是铁,所以B是硝酸铁,C是硝酸亚铁,B的化学式是Fe(NO3)3,反应②的离子方程式为2Fe3+ +Fe=3Fe2+。
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则A是H2S,B是S,C是SO2,D是氧气,因此反应③的化学方程式为2H2S+SO2=3S+2H2O;
(5)若A、B、C的水溶液均显碱性,焰色反应均为黄色,D为CO2,则A是氢氧化钠,B是碳酸钠,C是碳酸氢钠,碳酸根水解显碱性,离子方程式为CO32-+H2O![]() HCO3-+OH-;碳酸氢钠的主要用途有治疗胃酸过多、发酵粉、泡沫灭火器等。
HCO3-+OH-;碳酸氢钠的主要用途有治疗胃酸过多、发酵粉、泡沫灭火器等。

 阅读快车系列答案
阅读快车系列答案