题目内容
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是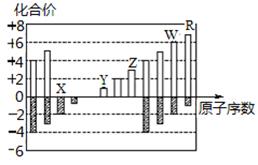
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R>W |
| C.WX3和水反应形成离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物不能相互反应 |
B
解析试题分析:结合化合价与原子序数的关系,判断X、Y、Z、W、R分别是O、Na、Al、S、Cl元素。A、Na、Al的电子层数相同,核电荷数多的半径小,所以原子半径:Y>Z>X,错误;B、S、Cl中非金属性强的是Cl,所以气态氢化物的稳定性:R>W,正确;C、WX3和水反应形成硫酸,是共价化合物,错误; D、
Y和Z两者最高价氧化物对应的水化物分别是氢氧化钠、氢氧化铝,二者能发生反应,错误,答案选B。
考点:考查利用元素化合价判断元素的种类,元素周期律的应用

练习册系列答案
相关题目
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.微粒X2-与Y2+核外电子排布相同,离子半径:X2-> Y2+ |
| B.人们可在周期表的过渡元素中寻找催化剂、耐腐蚀和耐高温的合金材料 |
| C.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F |
| D.Be元素与Al元素同处在周期表的金属与非金属的交界处,可推出: |
与氢氧根具有相同的质子数和电子数的微粒是
| A.CH4 | B.NH4+ | C.NH2- | D.Cl- |
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A.离子半径:C>D>B>A | B.原子序数:d>c>b>a |
| C.原子半径:A>B>C>D | D.单质的还原性:A>B>D>C |
甲、乙是周期表中同一主族的两种元素,若甲的原子序数为X,则乙的原子序数不可能为 ( )
| A.X+32 | B.X+4 | C.X+8 | D.X+18 |
在一定条件下,RO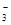 与R-可发生反应:RO
与R-可发生反应:RO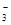 +5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
+5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
| A.元素R位于周期表中第ⅤA族 |
B.RO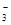 中的R只能被还原 中的R只能被还原 |
| C.CaR2是离子化合物,阴阳离子电子层结构相同,且既含有离子键,又含有共价键 |
| D.3 mol R2中,氧化产物与还原产物的质量比为5︰1 |
下列元素中,不属于主族元素的是( )
| A.钡 | B.铁 | C.钙 | D.碘 |