题目内容
天然气的主要成分是甲烷.在某平衡体系中存在CH4、H2O、CO、H2四种气体,其平衡常数表达式为k=
.已知温度、压强和水碳比[
]对甲烷转化反应的影响如图:
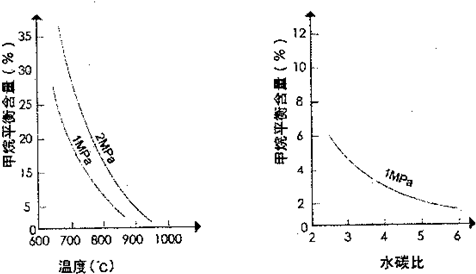
请回答下列问题:
(1)写出该可逆反应的化学方程式:
(2)根据图判断△H
(3)假设上述反应在恒容、恒温下进行,判断反应达到平衡状态时的标志是
A.CO减少的化学反应速率和H2O减少的化学反应速率相等
B.CO、H2O(g)、CH4、H2的浓度都相等
C.CO、H20(g)、CH4、H2的浓度都不再发生变化
D.正、逆反应速率都为零
(4)在图画出压强为2MPa时,CH4平衡含量与水碳比之间关系曲线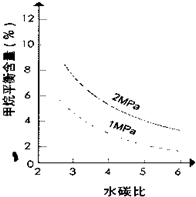
 .
.
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| n(H2O) |
| n(CH4) |

请回答下列问题:
(1)写出该可逆反应的化学方程式:
CH4(g)+H2O(g)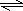 CO(g)+3H2(g)
CO(g)+3H2(g)
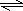 CO(g)+3H2(g)
CO(g)+3H2(g)CH4(g)+H2O(g)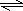 CO(g)+3H2(g)
CO(g)+3H2(g)
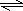 CO(g)+3H2(g)
CO(g)+3H2(g)(2)根据图判断△H
>
>
0,△S>
>
0(选填“>”、“<”或“=”).(3)假设上述反应在恒容、恒温下进行,判断反应达到平衡状态时的标志是
AC
AC
A.CO减少的化学反应速率和H2O减少的化学反应速率相等
B.CO、H2O(g)、CH4、H2的浓度都相等
C.CO、H20(g)、CH4、H2的浓度都不再发生变化
D.正、逆反应速率都为零
(4)在图画出压强为2MPa时,CH4平衡含量与水碳比之间关系曲线


分析:(1)根据平衡常数可知,反应中CO和H为生成物,CH4和H2O为反应,以此书写反应的化学方程式;
(2)根据平衡移动曲线的变化特点判断反应热,根据混乱度的变化来判断熵变;
(3)根据化学平衡为动态平衡,达到平衡时正逆反应速率相等,各物质的浓度不再发生改变来判断平衡状态;
(4)根据压强增大平衡向逆反应方向移动来画出曲线.
(2)根据平衡移动曲线的变化特点判断反应热,根据混乱度的变化来判断熵变;
(3)根据化学平衡为动态平衡,达到平衡时正逆反应速率相等,各物质的浓度不再发生改变来判断平衡状态;
(4)根据压强增大平衡向逆反应方向移动来画出曲线.
解答:解:(1)根据平衡常数可知,反应中CO和H为生成物,CH4和H2O为反应,
反应的化学方程式为CH4(g)+H2O(g)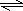 CO(g)+3H2(g),
CO(g)+3H2(g),
故答案为:CH4(g)+H2O(g)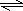 CO(g)+3H2(g);
CO(g)+3H2(g);
(2)根据图象中曲线的变化趋势可知,当温度升高时,甲烷的百分含量减小,说明升高温度平衡向逆反应方向移动,则正反应吸热,△H>0,生成物气体的物质的量大于反应物气体的物质的量,混乱度增大,则△S>0,
故答案为:>;>;
(3)A.CO减少的化学反应速率和H2O减少的化学反应速率相等,说明正逆反应速率相等,达到平衡状态,故A正确;
B.CO、H2O(g)、CH4、H2的浓度都相等,不能说明达到平衡状态,平衡时各物质的浓度取决于反应时各种物质的配比数和反应的程度,故B错误;
C.CO、H20(g)、CH4、H2的浓度都不再发生变化,说明达到平衡状态,故C正确;
D.正、逆反应速率都为零,不正确,化学平衡为动态平衡,平衡时正逆反应速率相等,不为0,故D错误.
故答案为:AC;
(4)压强增大,平衡向逆反应方向移动,甲烷的平衡含量减小,故答案为:
反应的化学方程式为CH4(g)+H2O(g)
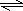 CO(g)+3H2(g),
CO(g)+3H2(g),故答案为:CH4(g)+H2O(g)
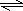 CO(g)+3H2(g);
CO(g)+3H2(g);(2)根据图象中曲线的变化趋势可知,当温度升高时,甲烷的百分含量减小,说明升高温度平衡向逆反应方向移动,则正反应吸热,△H>0,生成物气体的物质的量大于反应物气体的物质的量,混乱度增大,则△S>0,
故答案为:>;>;
(3)A.CO减少的化学反应速率和H2O减少的化学反应速率相等,说明正逆反应速率相等,达到平衡状态,故A正确;
B.CO、H2O(g)、CH4、H2的浓度都相等,不能说明达到平衡状态,平衡时各物质的浓度取决于反应时各种物质的配比数和反应的程度,故B错误;
C.CO、H20(g)、CH4、H2的浓度都不再发生变化,说明达到平衡状态,故C正确;
D.正、逆反应速率都为零,不正确,化学平衡为动态平衡,平衡时正逆反应速率相等,不为0,故D错误.
故答案为:AC;
(4)压强增大,平衡向逆反应方向移动,甲烷的平衡含量减小,故答案为:

点评:本题考查化学平衡移动以及平衡移动图象问题,题目难度不大,本题注意把握如何判断平衡状态的标志问题.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
① CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
② CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
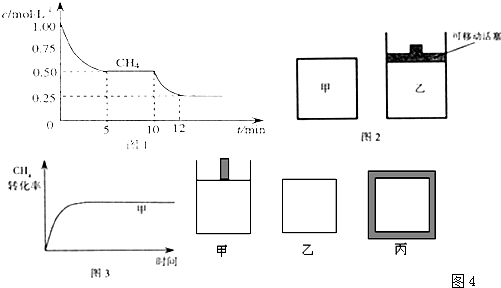
⑴ 在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。反应进行的前5 min内, v(H2)= ▲ ;10 min时,改变的外界条件可能是 ▲ 。
|

⑵ 如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像。

⑶ 反应③中ΔH3= ▲ 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应③中正、逆反应速率的关系式是 ▲ (填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断



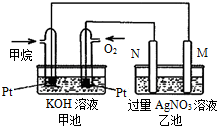 天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.
天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.