��Ŀ����
����Ŀ����2L����ѹ�Ƶĺ����ܱ�������ͨ��2 molX(g)��1molY(g)��������Ӧ��2X(g)��Y(g)![]() 2Z(g) ��H<0�����ﵽƽ��ʱ���������ʵ�����Ϊԭ����0.85������ش��������⡣
2Z(g) ��H<0�����ﵽƽ��ʱ���������ʵ�����Ϊԭ����0.85������ش��������⡣
��1������Ӧ����5min�ﵽƽ�⣬��Y��ƽ����Ӧ����Ϊ__��
��2����ͬ�����½��з�Ӧ����t1ʱ�̣�ֻ�ı�����ijһ��������������ͼ����ͼ�ס�

��n��0.9mol��t1ʱ�̸ı��������__(��ѡ���ţ�A.���� B.���� C.��ѹ D.��ѹ E.�Ӵ���)��t2__5min(��������������������������ͬ)��
��3���������������䣬ԭ����Ϊ��ѹ�������ﵽƽ���Z�����ʵ���__0.9mol��
��4���������ʵ�����Ϊ3mol������X��Y�����5L�����з�����Ӧ���ڷ�Ӧ������Z�����ʵ����������¶ȱ仯��ͼ�ҡ�
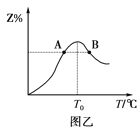
��A��B����Z��������Ӧ���ʵĴ�С��ϵ��__����������A��B��ʾ��
���¶�T<T0ʱ��Z%�������ԭ����___��
���𰸡�0.045 mol��L-1��min-1 E �� �� B��A ��Ӧ��û�дﵽƽ�⣬��Ӧ������Ӧ������У���Z%������
��������
��2L����ѹ�Ƶĺ����ܱ�������ͨ��2 molX(g)��1molY(g)��������Ӧ��
2X(g) ��Y(g)![]() 2Z(g)
2Z(g)
��ʼ 1 mol��L-1 0.5 mol��L-1 0
ת�� 2x x 2x
ƽ�� 1-2x 0.5-x 2x
�ﵽƽ��ʱ���������ʵ�����Ϊԭ����0.85������![]() ��x=0.225 mol��L-1���ﵽƽ��״̬ʱ��Z�����ʵ�����0.9mol������Ӱ�췴Ӧ���ʺ�ƽ���ƶ������ػش�
��x=0.225 mol��L-1���ﵽƽ��״̬ʱ��Z�����ʵ�����0.9mol������Ӱ�췴Ӧ���ʺ�ƽ���ƶ������ػش�
��1���������������� 5min��Y��Ũ�ȱ仯Ϊ0.225 mol��L-1����Y��ƽ����Ӧ����Ϊ![]() 0.045 mol��L-1��min-1��
0.045 mol��L-1��min-1��
��2����ͼ���֪����t1ʱ�̣��ı�������Ӧ���ʼӿ죬��n��0.9mol��˵��ƽ�ⲻ�ƶ��� A.������Ӧ���ȣ�����ƽ�������ƶ���Z�����ʵ�����С���ʲ�ѡA��
B. .������Ӧ���ȣ����·�Ӧ���ʼ�������ƽ�������ƶ���Z�����ʵ������ʲ�ѡB�� C. ������Ӧ�������ʵ�����С����ѹƽ�������ƶ���Z�����ʵ������ʲ�ѡC��
D.������Ӧ�������ʵ�����С����ѹƽ�������ƶ���Z�����ʵ�����С���ҷ�Ӧ���ʼ������ʲ�ѡD�� E.�Ӵ�������Ӧ���ʼӿ졢ƽ�ⲻ�ƶ�����ѡE��
ƽ�ⲻ�ƶ�����Ӧ���ʼӿ죬�ﵽƽ���ʱ�����̣�����t2��5min��
��3��������Ӧ�������ʵ�����С���������������䣬ԭ����Ϊ��ѹ�������൱�ڼ�ѹ��ƽ�������ƶ����ﵽƽ���Z�����ʵ�����0.9mol��
��4�����¶�Խ�ߣ���Ӧ����Խ�죬B����¶ȴ���A������A��B����Z��������Ӧ���ʵĴ�С��ϵ��B��A��
���¶�T��T0ʱ����Ӧ��û�дﵽƽ�⣬��Ӧ������Ӧ������У�����Z%������