题目内容
【题目】能证明碳酸比硅酸酸性强的实验事实是( )
A. CO2是气体,而SiO2是固体 B. 高温下能反应 Na2CO3+SiO2=Na2SiO3+CO2↑
C. CO2溶于水生成碳酸,而SiO2却不溶于水 D. CO2通入Na2SiO3溶液中有胶状沉淀生成
【答案】D
【解析】A、氧化物的状态不能决定氧化物水化物的酸性强弱,故A错误;B、反应原理是高沸点制低沸点气体,之所以能发生是因为生成了挥发性的气体二氧化碳,故B错误;C、氧化物的水溶性不能决定其水化物的酸性强弱,故C错误;D、CO2+H2O+Na2SiO3═Na2CO3+H2SiO3↓,强酸能制弱酸,所以酸性:碳酸>硅酸,故D正确。故选D。

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
【题目】下列反应中,相关坐标图像错误的是( )
的是
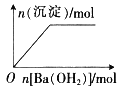
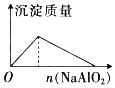
A | B | C | D |
NaHSO4溶液中逐滴加入Ba(OH)2 溶液 | 向盐酸中滴入NaAlO2溶液 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
A. AB. BC. CD. D