题目内容
红矾钠(重铬酸钠:Na2Cr2O7?2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛.
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO?Cr2O3)利用以下过程来制取.
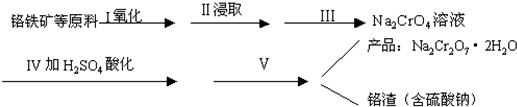
①步骤I中反应的化学方程式为:
4FeO?Cr2O3(s)+8Na2CO3(s)+7O2?8Na2CrO4(s)+2Fe2O3(s)+8CO2;△H<0
该反应的化学平衡常数的表达式为
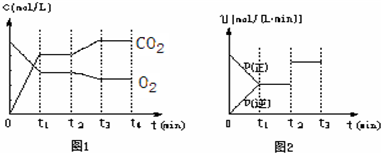
②图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
由图1判断,反应进行至t2min时,曲线发生变化的原因是
由图2判断,t2min到t3 min 的曲线变化的原因可能是
a.升高温度 b.加了催化剂 c.将原料粉碎 d.缩小容器体积
(2)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是
①步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是
②步骤Ⅳ中发生反应的离子方程式为:
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO?Cr2O3)利用以下过程来制取.

①步骤I中反应的化学方程式为:
4FeO?Cr2O3(s)+8Na2CO3(s)+7O2?8Na2CrO4(s)+2Fe2O3(s)+8CO2;△H<0
该反应的化学平衡常数的表达式为
K=
| c(CO2)8 |
| c(O2)7 |
K=
.| c(CO2)8 |
| c(O2)7 |
②图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
由图1判断,反应进行至t2min时,曲线发生变化的原因是
t2时对平衡体系降温
t2时对平衡体系降温
(用文字表达).由图2判断,t2min到t3 min 的曲线变化的原因可能是
b
b
(填编号)a.升高温度 b.加了催化剂 c.将原料粉碎 d.缩小容器体积

(2)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是
Na[A1(OH)4](或NaA1O2)
Na[A1(OH)4](或NaA1O2)
、Na2SiO3
Na2SiO3
.①步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是
除去[A1(OH)4]-(或A1O2-)、SiO32-等杂质
除去[A1(OH)4]-(或A1O2-)、SiO32-等杂质
.②步骤Ⅳ中发生反应的离子方程式为:
2CrO42-+2H+=Cr2O72-+H2O
2CrO42-+2H+=Cr2O72-+H2O
.分析:(1)①根据平衡常数表达式的含义和书写方法来回答;
②由图1判断,反应进行至t2min时,二氧化碳的浓度均在原来基础上减小,氧气的浓度在原来基础上是增大的,一定不是二者的浓度变化导致的;由图2判断,t2min到t3min 正逆反应速率仍相等,化学平衡不移动;
(2)根据铬铁矿中含有Al2O3、MgO、SiO2等杂质所发生的反应来回答;
①将溶液的pH调至7~8并煮沸,可以将一部分杂质离子除去;
②CrO42-在酸性环境下可以转化为重铬酸根.
②由图1判断,反应进行至t2min时,二氧化碳的浓度均在原来基础上减小,氧气的浓度在原来基础上是增大的,一定不是二者的浓度变化导致的;由图2判断,t2min到t3min 正逆反应速率仍相等,化学平衡不移动;
(2)根据铬铁矿中含有Al2O3、MgO、SiO2等杂质所发生的反应来回答;
①将溶液的pH调至7~8并煮沸,可以将一部分杂质离子除去;
②CrO42-在酸性环境下可以转化为重铬酸根.
解答:解:(1)①根据平衡常数表达式=
,所以K=
,故答案为:K=
;
②由图1判断,反应进行至t2min时,二氧化碳的浓度均在原来基础上减小,氧气的浓度在原来基础上是增大的,说明平衡正向移动,可以是降低温度,故答案为:t2 时对平衡体系降温;由图2判断,t2min到t3 min 正逆反应速率加快并且仍相等,化学平衡不移动,则一定是加入了催化剂,故答案为:b;
(2)铬铁矿的主要成份为FeO?Cr2O3,还含有Al2O3、MgO、SiO2等杂质,当加入纯碱氧化的过程中,发生副反应:SiO2+Na2CO3
Na2SiO3+CO2↑、Al2O3+Na2CO3
2NaAlO2+CO2↑,故答案为:Na[A1(OH)4](或NaA1O2)、Na2SiO3;
①将溶液的pH调至7~8并煮沸,可以将[A1(OH)4]-(或A1O2-)、SiO32-等离子转化为沉淀而除去,故答案为:除去[A1(OH)4]-(或A1O2-)、SiO32-等杂质;
②CrO42-在酸性环境下可以转化为重铬酸根,即2CrO42-+2H+=Cr2O72-+H2O,故答案为:2CrO42-+2H+=Cr2O72-+H2O.
| 各个生成物平衡浓度的系数次方的乘积 |
| 各个反应物平衡浓度系数次方的乘积 |
| c(CO2)8 |
| c(O2)7 |
| c(CO2)8 |
| c(O2)7 |
②由图1判断,反应进行至t2min时,二氧化碳的浓度均在原来基础上减小,氧气的浓度在原来基础上是增大的,说明平衡正向移动,可以是降低温度,故答案为:t2 时对平衡体系降温;由图2判断,t2min到t3 min 正逆反应速率加快并且仍相等,化学平衡不移动,则一定是加入了催化剂,故答案为:b;
(2)铬铁矿的主要成份为FeO?Cr2O3,还含有Al2O3、MgO、SiO2等杂质,当加入纯碱氧化的过程中,发生副反应:SiO2+Na2CO3
| ||
| ||
①将溶液的pH调至7~8并煮沸,可以将[A1(OH)4]-(或A1O2-)、SiO32-等离子转化为沉淀而除去,故答案为:除去[A1(OH)4]-(或A1O2-)、SiO32-等杂质;
②CrO42-在酸性环境下可以转化为重铬酸根,即2CrO42-+2H+=Cr2O72-+H2O,故答案为:2CrO42-+2H+=Cr2O72-+H2O.
点评:本题是一道化学平衡常数和影响化学反应速率的因素的一道综合题,注意利用习题中的信息来解答,题目难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

 Cr2O72-+H2O
Cr2O72-+H2O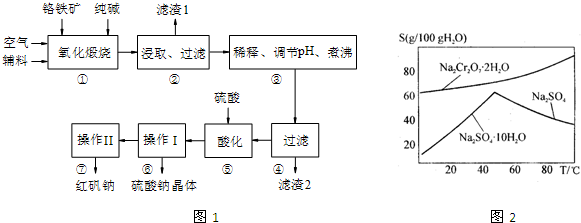
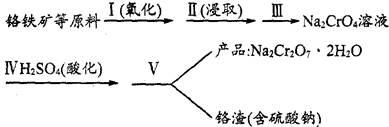
 8Na2CrO4(s)+2Fe2O3(s)+8CO2,该反应的化学平衡常数的表达式为)_____________,在常温下该反应速率极慢,下列措施中不能使反应速率增大的是____________ 。
8Na2CrO4(s)+2Fe2O3(s)+8CO2,该反应的化学平衡常数的表达式为)_____________,在常温下该反应速率极慢,下列措施中不能使反应速率增大的是____________ 。