题目内容
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A、反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B、在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3给出孤对电子 |
| C、向反应后的溶液加入乙醇,溶液没有发生变化 |
| D、沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
考点:配合物的成键情况,铜金属及其重要化合物的主要性质
专题:化学键与晶体结构,元素及其化合物
分析:氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液.
A.硫酸铜先和氨水反应生成氢氧化铜,氢氧化铜和氨水反应生成络合物;
B.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键;
C.络合物在乙醇中溶解度较小,所以会析出;
D.氢氧化铜和氨水反应生成配合物而使溶液澄清;
A.硫酸铜先和氨水反应生成氢氧化铜,氢氧化铜和氨水反应生成络合物;
B.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键;
C.络合物在乙醇中溶解度较小,所以会析出;
D.氢氧化铜和氨水反应生成配合物而使溶液澄清;
解答:
解:A.硫酸铜和氨水反应生成氢氧化铜蓝色沉淀,继续加氨水时,氢氧化铜和氨水继续反应生成络合物而使溶液澄清,所以溶液中铜离子浓度减小,故A错误.
B.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对,故B正确;
C.[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,向溶液中加入乙醇后会析出蓝色晶体,故C错误;
D.硫酸铜和氨水反应生成氢氧化铜蓝色沉淀,继续加氨水时,氢氧化铜和氨水继续反应生成络合物离子[Cu(NH3)4]2+而使溶液澄清,故D正确;
故选BD
B.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对,故B正确;
C.[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,向溶液中加入乙醇后会析出蓝色晶体,故C错误;
D.硫酸铜和氨水反应生成氢氧化铜蓝色沉淀,继续加氨水时,氢氧化铜和氨水继续反应生成络合物离子[Cu(NH3)4]2+而使溶液澄清,故D正确;
故选BD
点评:本题考查了配合物、配位键的形成等性质,难度不大,明确形成配合物的条件是:有提供空轨道的中心原子,有提供孤电子对的配位体.

练习册系列答案
相关题目
在某无色透明溶液中,下列离子能大量共存的是( )
| A、Na+、Mg2+、Cl-、OH- |
| B、H+、Cu2+、NO3-、SO42- |
| C、Mg2+、SO42-、K+、NO3- |
| D、Na+、MnO4-、Ca2+、CO32- |
下列粒子(或化学键)的数目之比不是1:1的是( )
| A、氘原子中的质子和中子 |
| B、Na2O2固体中的阴离子和阳离子 |
| C、CO2分子中的σ键和π键 |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH- |
下列表述正确的是( )
| A、醛基的结构简式-COH |
B、聚丙烯的结构简式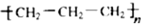 |
C、四氯化碳分子的电子式 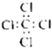 |
D、丙烷分子的球棍模型 |
下列反应属于取代反应的是( )
| A、乙醇和浓硫酸混合加热至170℃ |
| B、苯和液溴混合后加入少量铁屑 |
| C、甲苯与酸性高锰酸钾溶液混合 |
| D、乙烯通入酸性高锰酸钾溶液中 |
下列说法中,正确的是( )
| A、HCl和H2SO4属于同类化合物,但它们在水溶液里电离时生成有不同的阴离子,所以它们的化学性质有所不同 |
| B、无氧酸的正盐一定不含氢、氧元素 |
| C、能电离产生氢离子的化合物一定属于酸 |
| D、将Cu(OH)2加入到滴有石蕊试液的蒸馏水中,溶液呈蓝色 |
在2L密闭容器中,在一定条件下发生A(g)+3B(g)?2C(g),在10s内反应物A的浓度由1mol/L降到0.4mol/L,则ν(C)为( )
| A、0.06mol/(L?s) |
| B、0.12mol/(L?s) |
| C、0.6mol/(L?s) |
| D、1.2mol/(L?s) |