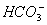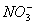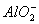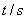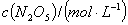题目内容
下列说法正确的是
A. 相同温度下,1 mol·L-1氨水溶液与0.5 mol·L-1氨水溶液中,c(OH-)之比是2:1
B. 0.1 mol·L-1 NH4Cl溶液中的c(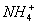 )=c(
)=c(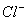 )
)
C. 向0.1 mol·L-1NaNO3 溶液中滴加稀盐酸,使溶液pH=1,此时混合液中c(Na+)=c(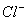 )
)
D. 向醋酸钠溶液中加入适量醋酸,使 混合液的pH=7,此时混合液中c(Na+)=c(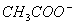 )
)
【解析】A项中如果是强碱,其浓度之比与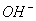 浓度之比相等,但此处氨水是弱碱,稀氨水的电离程度大,所以二者的
浓度之比相等,但此处氨水是弱碱,稀氨水的电离程度大,所以二者的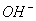 浓度之比小于2:1;B项中如果是强酸强碱盐,不发生水解,则等式成立,但NH4Cl中的
浓度之比小于2:1;B项中如果是强酸强碱盐,不发生水解,则等式成立,但NH4Cl中的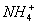 水解后,消耗OH-、积累H+,c(
水解后,消耗OH-、积累H+,c(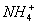 )<c(
)<c(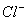 )。C项中NaNO3和HCl都是强电解质,完全电离为离子,满足己知条件要求。D项中pH=7,c(H+)=C(
)。C项中NaNO3和HCl都是强电解质,完全电离为离子,满足己知条件要求。D项中pH=7,c(H+)=C(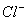 ),根据电荷守恒:C(H+)+C(Na+)=C(
),根据电荷守恒:C(H+)+C(Na+)=C(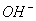 )+C(
)+C(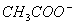 ),即得答案。
),即得答案。
【答案】CD

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
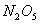 是一种新型硝化剂,在一定温度下可发生以下反应:
是一种新型硝化剂,在一定温度下可发生以下反应:
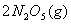

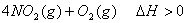
 温度时,向密闭容器中通入
温度时,向密闭容器中通入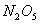 ,部分实验数据见下表:
,部分实验数据见下表:
|
| 0 | 500 | 1000 | 1500 |
|
| 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是( )
A. 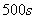 内
内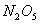 分解速率为
分解速率为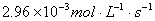
B.  温度下的平衡常数
温度下的平衡常数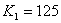 ,平衡时
,平衡时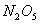 的转化率为50%
的转化率为50%
C.  温度下的平衡常数为
温度下的平衡常数为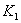 ,
,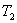 温度下的平衡常数为
温度下的平衡常数为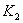 ,若
,若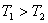 ,则
,则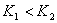
D. 达平衡后其他条件不变,将容器的体积压缩到原来的 ,则再次平衡时
,则再次平衡时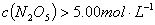
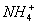
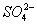
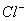 B.Na+ Mg2+
B.Na+ Mg2+