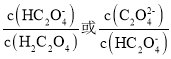题目内容
【题目】控制适合的条件,将反应2Fe3++2I-![]() 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是( )
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是( )
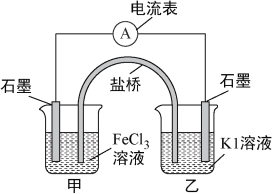
A. 反应开始时,乙中石墨电极上发生氧化反应
B. 反应开始时,甲中石墨电极上Fe3+被还原
C. 电流计读数为零时,反应达到化学平衡状态
D. 电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
【答案】D
【解析】
由反应2Fe3+ +2I- ![]() 2Fe2+ +I2可知,反应开始时,甲中Fe3+发生还原反应,乙中I-发生氧化反应;当电流计读数为零时,则反应达到了平衡状态,此时在甲中溶入FeCl2固体,平衡向逆反应方向移动,乙中I2发生还原反应,则乙中石墨电极为正极。
2Fe2+ +I2可知,反应开始时,甲中Fe3+发生还原反应,乙中I-发生氧化反应;当电流计读数为零时,则反应达到了平衡状态,此时在甲中溶入FeCl2固体,平衡向逆反应方向移动,乙中I2发生还原反应,则乙中石墨电极为正极。
A.反应开始时乙中石墨电极上I-被氧化成I2,发生了氧化反应,故A正确。B.反应开始时,甲中石墨电极上Fe3+被还原成Fe2+,故正B确;C.当电流计读数为零时,则反应达到了平衡状态,故C正确。D. 电流计读数为零后,在甲中溶入FeCl2固体,则甲中Fe2+浓度变大,发生氧化反应,甲为负极,故D错误。答案:D。

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】实验室制备1,2-二溴乙烷的反应中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | -1l6 |
回答下列问题:
(1)在此实验中,反应方程式为:_________;________。
(2)要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)在装置C中应加入_______,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)若产物中有少量未反应的Br2,最好用_________洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(5)判断该制备反应已经结束的最简单方法是_____________;
(6)反应过程中应用冷水冷却装置D,其主要目的是________________;但又不能过度冷却(如用冰水),其原因是_____________________。