题目内容
交通警察执法时常使用的便携式酒精检查仪可能应用了:3CH3CH2OH+2K2Cr2O7(橙色)+ 8H2SO4=3CH3COOH +2Cr2(SO4)3(蓝绿色)+2K2SO4+11H2O这一反应原理,关于该反应,下列说法正确的是( )
A. 该反应证明了,含最高价元素的化合物,一定具有强氧化性
B. 1mol还原剂反应时,转移的电子数为2NA
C. H2SO4在反应中表现了氧化性和酸性
D. 可以利用该反应原理,将它设计成原电池,通过检测电流强度判断司机是否饮酒
练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
对下列实验现象的原因分析不正确的一项是( )
选项 | 实验现象 | 原因分析 |
A | 久置的浓硝酸呈黄色 | 浓硝酸不稳定,分解生成的NO2 溶解在其中 |
B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,呈酸性,使石蕊变红,HClO具有强氧化性、漂白性,使其褪色 |
C | SO2通入溴水中,溴水褪色 | SO2具有漂白性,使其褪色 |
D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
A. A B. B C. C D. D


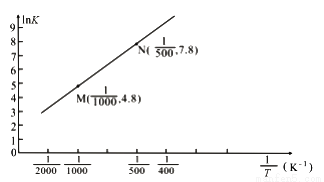
 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H 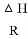 (气体常数R=8.3×10-3kJ·mol-1·K-1)。
(气体常数R=8.3×10-3kJ·mol-1·K-1)。