题目内容
【题目】向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g) 达到平衡,正反应速率随时间变化的示意图如下所示,由图可得出的正确结论是
SO3(g)+NO(g) 达到平衡,正反应速率随时间变化的示意图如下所示,由图可得出的正确结论是
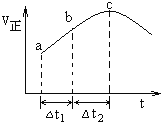
A. 反应在c点达到平衡状态
B. △t1=△t2时,SO2的转化率:a~b段小于b~c段
C. 反应物浓度:a点小于b点
D. 反应物的总能量低于生成物的总能量
【答案】B
【解析】分析:反应开始时反应物浓度最大,但正反应速率逐渐增大,说明该反应为放热反应,温度升高,正反应速率增大,随着反应的进行,反应物浓度逐渐减小,正反应速率也逐渐减小。
详解:A. 当正反应速率不变时,才能说明反应达到平衡状态,虽然c点时正反应速率最大,但c点后正反应速率减小,反应继续向正反应方向进行,没有达到平衡状态,故A错误;
B. a点到c点,正反应速率增大,消耗SO2的物质的量增大,即SO2转化率增大,所以△t1=△t2时,SO2的转化率:a~b段小于b~c段,故B正确;
C. a点到b点时,反应向正反应方向进行,反应物浓度逐渐降低,所以反应物浓度:a点大于b点,故C错误;
D. 由上述分析可知,该反应为放热反应,则反应物总能量大于生成物总能量,故D错误;答案选B。

 名题金卷系列答案
名题金卷系列答案【题目】X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2 , 且原子半径是同族元素中最小的.
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有1个未成对电子.
③Z元素的电离能数据见表(kJ/mol):
I1 | I2 | I3 | I4 | … |
496 | 4562 | 6912 | 9540 | … |
请回答:
(1)Z2Y2的电子式为 , 含有的化学键类型 , Z2Y2为晶体.
(2)X、Y、Z三种元素所形成的常见化合物的名称为;XY2的结构式为 , 分子立体构型为 .
(3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是(填名称);晶体ZW的熔点比晶体XW4明显高的原因是 .