题目内容
【题目】同温同压下,同体积的CO和CO2,下列说法不正确的是( )
A.分子数之比等于1:1B.碳原子数之比等于2:3
C.物质的量之比等于1:1D.原子数之比等于2:3
【答案】B
【解析】
A. 根据阿伏加德罗定律,同温同压下,同体积的CO和CO2,分子数相同,所以分子数之比等于1:1,故A正确;
B. 同温同压下,同体积的CO和CO2,分子数之比等于1:1,所以碳原子数之比等于1:1,故B错误;
C. 根据阿伏加德罗定律,同温同压下,同体积的CO和CO2,物质的量一定相同,故C正确;
D. 根据阿伏加德罗定律,同温同压下,同体积的CO和CO2,物质的量一定相同,原子数之比等于2:3,故D正确;
答案选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】有Ⅰ、Ⅱ、Ⅲ3个体积均为0.5L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)△H。HCl的平衡转化率与Z和T的关系如图所示。
2Cl2(g)+2H2O(g)△H。HCl的平衡转化率与Z和T的关系如图所示。
容器 | 起始时 | ||
T/℃ | n(HCl)/mol | Z | |
Ⅰ | 300 | 0.25 | a |
Ⅱ | 300 | 0.25 | b |
Ⅲ | 300 | 0.25 | 4 |
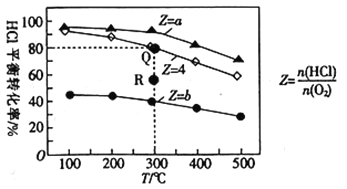
下列说法不正确的是( )
A. △H<0
B. a<4<b
C. 若容器Ⅲ反应某时刻处于R点,则R点的反应速率:v(正)>v(逆)
D. 300℃时,该反应平衡常数的值为320