题目内容
写出下列反应的离子方程式:
①氢氧化钙溶液与少量NaHCO3反应 ;
②铝和氢氧化钠溶液反应 ;
③在饱和的Na2CO3溶液通入CO2 ;
④向AlCl3溶液中加入过量NaOH溶液 ;
⑤向NaAlO2溶液中逐滴少量盐酸 .
①氢氧化钙溶液与少量NaHCO3反应
②铝和氢氧化钠溶液反应
③在饱和的Na2CO3溶液通入CO2
④向AlCl3溶液中加入过量NaOH溶液
⑤向NaAlO2溶液中逐滴少量盐酸
考点:离子方程式的书写
专题:离子反应专题
分析:①少量NaHCO3完全反应,生成碳酸钙、水、NaOH;
②反应生成偏铝酸钠和氢气;
③反应生成碳酸氢钠,析出晶体;
④加入过量NaOH溶液,反应生成偏铝酸钠;
⑤滴少量盐酸,反应生成氢氧化铝沉淀.
②反应生成偏铝酸钠和氢气;
③反应生成碳酸氢钠,析出晶体;
④加入过量NaOH溶液,反应生成偏铝酸钠;
⑤滴少量盐酸,反应生成氢氧化铝沉淀.
解答:
解:①少量NaHCO3完全反应,生成碳酸钙、水、NaOH,离子反应为HCO3-+0H-+Ca2+═CaCO3↓+H2O,故答案为:HCO3-+0H-+Ca2+═CaCO3↓+H2O;
②反应生成偏铝酸钠和氢气,离子反应为2Al+20H-+H2O=2Al02-+3H2↑,故答案为:2Al+20H-+H2O=2Al02-+3H2↑;
③反应生成碳酸氢钠,析出晶体,离子反应为2Na++CO32-+CO2+H2O=2NaHCO3↓,故答案为:2Na++CO32-+CO2+H2O=2NaHCO3↓;
④加入过量NaOH溶液,反应生成偏铝酸钠,离子反应为Al3++40H-═AlO2-+2H2O,故答案为:Al3++40H-═AlO2-+2H2O;
⑤滴少量盐酸,反应生成氢氧化铝沉淀,离子反应为H++AlO2-+H2O=Al(OH)3↓,故答案为:H++AlO2-+H2O=Al(OH)3↓.
②反应生成偏铝酸钠和氢气,离子反应为2Al+20H-+H2O=2Al02-+3H2↑,故答案为:2Al+20H-+H2O=2Al02-+3H2↑;
③反应生成碳酸氢钠,析出晶体,离子反应为2Na++CO32-+CO2+H2O=2NaHCO3↓,故答案为:2Na++CO32-+CO2+H2O=2NaHCO3↓;
④加入过量NaOH溶液,反应生成偏铝酸钠,离子反应为Al3++40H-═AlO2-+2H2O,故答案为:Al3++40H-═AlO2-+2H2O;
⑤滴少量盐酸,反应生成氢氧化铝沉淀,离子反应为H++AlO2-+H2O=Al(OH)3↓,故答案为:H++AlO2-+H2O=Al(OH)3↓.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
下列相关表达正确的是( )
| A、亚硫酸的电离方程式:H2SO3=2H++SO2-3 | ||
B、中子数为18的氯原子的原子符号:
| ||
| C、(CH3)2CHCH2CH2OH的名称:3-甲基-1-丁醇 | ||
D、HOCH2COOH缩聚产物的结构简式: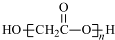 |
某有机物中间体结构如图所示,它不能发生的反应类型是( )
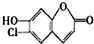

| A、加成反应 | B、取代反应 |
| C、水解反应 | D、消去反应 |
设NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、1mol CH4(g)和2mol O2(g)的能量总和小于1mol CO2(g)和2mol H2O(g)的能量总和 |
| B、标准状况下,44.8L NO与22.4L O2混合后气体中分子总数小于2NA |
| C、1mol Fe在氧气中充分燃烧失去3NA个电子 |
| D、在标准状况下,NA个CHCl3分子所占的体积约为22.4L |
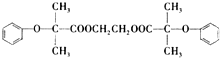 )可由下列路线合成:
)可由下列路线合成: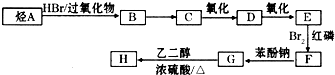

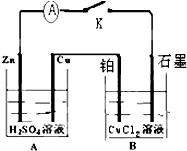 如图,回答问题:
如图,回答问题: