题目内容
【题目】已知反应:①![]()
![]() ,②
,②![]()
![]() 。下列结论正确的是
。下列结论正确的是
A.碳的燃烧热大于110.5 kJ·mol1
B.①的反应热为221 kJ·mol1
C.浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量
【答案】A
【解析】
A. 根据①反应,2mol碳(s)反应生成CO(g)放出221kJ的热量,生成CO2(g)放出热量大于221kJ,因此碳的燃烧热大于110.5 kJ·mol1,故A正确;
B. ①的反应热为-221 kJ·mol1,故B错误;
C. 浓硫酸溶于水会放出大量热,因此浓硫酸与稀NaOH溶液反应生成1mol水,放出热量大于57.3 kJ,故C错误;
D. 醋酸电离会吸收热量,因此稀醋酸与稀NaOH溶液反应生成1mol水,放出热量小于57.3 kJ,故D错误。
综上所述,答案为A。

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
【题目】已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
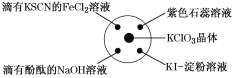
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变成蓝色 | Cl2具有氧化性 |
A.AB.BC.CD.D