题目内容
12.a g下列物质在氧气中充分燃烧后的气体(1.01×105Pa,120℃),通过足量的过氧化钠充分反应后,过氧化钠增重b g,符合b>a 的( )| A. | HCHO | B. | CH3OH | C. | HOOCCOOH | D. | 纤维素(C6H10O5)n |
分析 100度以上C、H、O化合物在氧气作用下,固体过氧化钠增重规律为:若分子组成满足(CO)n(H2)m的物质,固体增重等于自身质量;若多碳则会多增重,若多氧则会少增重.据此判断.
解答 解:A、HCHO可以改写出CO(H2),agHCHO充分燃烧后的气体通过足量过氧化钠,过氧化钠增重ag,故A不符合;
B、CH3OH可以改写出(CO)(H2)2,ag充分燃烧后的气体通过足量过氧化钠,过氧化钠增重ag,故B不符合;
C、HOOCCOOH可以改写出(CO)2(H2)O2,组成中氧原子增多,agHOOCCOOH充分燃烧后的气体通过足量过氧化钠,过氧化钠增重小于ag,故C不符合;
D、纤维素(C6H10O5)n改写出(CO)5n(H2)5nC,ag纤维素充分燃烧后的气体通过足量过氧化钠,过氧化钠增重大于ag,故D符合.
故选:D.
点评 本题考查根据反应方程式的计算,难度中等,关键根据反应方程式寻找质量变化,理解质量变化归纳总结规律,若分子组成满足(CO)n(H2)m的物质,固体增重等于自身质量;若多碳则会多增重,若多氧则会少增重.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
6.(Ⅰ)室温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?a=7时,HA是强酸;a>7时,HA是弱酸
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+)
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)=10-4-10-10mol/L.
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
H2B═H++HB- HB-?H++B2-
回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
( III)已知:25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9.
(6)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂.胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释)对于平衡BaSO4(s)?Ba2+(aq)+SO42-(aq),H+不能减少Ba2+或SO42-的浓度,平衡不能向溶解方向移动.
万一误服了少量BaCO3,应尽快用大量0.5mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为2×10-10mol/L.
| 实验 编号 | HA的物质的量 浓度(mol/L) | NaOH的物质的 量浓度(mol/L) | 混合后 溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(2)乙组混合溶液中c(A-)和c(Na+)的大小关系是C
A.前者大 B.后者大
C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+)
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)=10-4-10-10mol/L.
(Ⅱ)某二元酸(化学式用H2B表示)在水中的电离方程式是:
H2B═H++HB- HB-?H++B2-
回答下列问题:
(5)在0.1mol/L的Na2B溶液中,下列粒子浓度关系式正确的是AC.
A.c(B2-)+c(HB-)=0.1mol/L
B.c(B2-)+c(HB-)+c(H2B)=0.1mol/L
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
( III)已知:25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9.
(6)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂.胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释)对于平衡BaSO4(s)?Ba2+(aq)+SO42-(aq),H+不能减少Ba2+或SO42-的浓度,平衡不能向溶解方向移动.
万一误服了少量BaCO3,应尽快用大量0.5mol/L Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为2×10-10mol/L.
3.能正确表示下列反应的离子方程式是( )
| A. | 向NaOH溶液中通入过量的CO2:CO2+OH-═HCO3- | |
| B. | 将SO2气体通入Ba(NO3)2溶液:SO2+H2O+Ba2+═BaSO3↓+2H+ | |
| C. | 实验室制氯气:MnO2+4HCl(浓)═Mn2++2Cl2↑+2H2O | |
| D. | AlCl3溶液与过量氨水混合:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
17.下列溶液中Cl-的物质的量浓度与50mL 1mol/L FeCl3溶液中Cl-物质的量浓度相等是( )
| A. | 100 mL 1mol/L NaCl溶液 | B. | 75mL 1 mol/L MgCl2溶液 | ||
| C. | 150 mL 3mol/L KCl溶液 | D. | 25 mL 2 mol/L AlCl3溶液 |
1.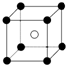 最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )
最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )
 最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )
最近发现一种由M、N原子构成的两种原子的气态团簇分子,如图所示.实心球“●”表示N原子,空心球“○”表示M原子,它的化学式为( )| A. | M4N4 | B. | MN8 | C. | MN | D. | M4N5 |
2.对于X+Y?Z的平衡,若增大压强,Y的转化率增大,则X和Z可能的状态是( )
| A. | X为液态,Z为气态 | B. | X为固态,Z为气态 | C. | X为气态,Z为气态 | D. | 无法确定 |