题目内容
现有下列短周期元素性质的数据:
下列说法正确的是( )
A. 第一电离能:① > ⑦ B. 电负性:② < ④
C. 相应离子的半径: ② >⑥> ①
D. 气态氢化物的稳定性和沸点:⑦﹤④
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高化合价 | | +2 | +1 | +5 | +7 | +1 | +5 |
| 最低化合物 | -2 | | | -3 | -1 | | -3 |
A. 第一电离能:① > ⑦ B. 电负性:② < ④
C. 相应离子的半径: ② >⑥> ①
D. 气态氢化物的稳定性和沸点:⑦﹤④
B
根据原子半径和最高最低化合价可以判断①是O;②是Mg;③是Li;④是P;⑤是Cl;⑥是Na;⑦是N;
A:N原子属于半充满状态,故第一电离能氮大于氧
B:镁为活泼金属,而P为非金属,电负性磷大于镁
C:三者离子的核外电子排布相同,核电荷数越大,离子半径越小,即:① >⑥> ②
D:N元素的非金属性强于P,故NH3稳定性强于与PH3;由于氨气分子间有氢键,故其沸点也相对较高
故答案为B
A:N原子属于半充满状态,故第一电离能氮大于氧
B:镁为活泼金属,而P为非金属,电负性磷大于镁
C:三者离子的核外电子排布相同,核电荷数越大,离子半径越小,即:① >⑥> ②
D:N元素的非金属性强于P,故NH3稳定性强于与PH3;由于氨气分子间有氢键,故其沸点也相对较高
故答案为B

练习册系列答案
相关题目
 (未完成)。
(未完成)。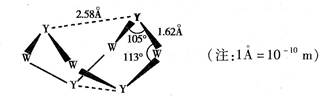
 。
。 为Y。在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X Y(填“>”、“=”或“<”)
为Y。在等体积、等pH的X、Y的溶液中分别加入等质量的锌粉,反应后若最后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X Y(填“>”、“=”或“<”)