��Ŀ����
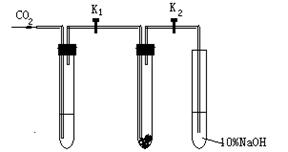
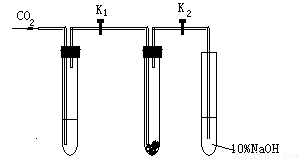
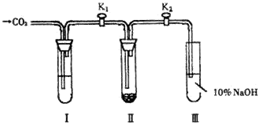 Ϊ��̽����������̼�Ƿ���ˮ����ʱ���ܺ������Ʒ�Ӧ���������о�С���ͬѧ���������ͼ��ʾ��ʵ��װ�ã��ֱ���мס�������ʵ�飺
Ϊ��̽����������̼�Ƿ���ˮ����ʱ���ܺ������Ʒ�Ӧ���������о�С���ͬѧ���������ͼ��ʾ��ʵ��װ�ã��ֱ���мס�������ʵ�飺ʵ��ף�����Ķ�����̼�������Ƶķ�Ӧ
�ڸ�����Թܢ���װ��Na2O2����ͨ��CO2֮ǰ���ر�K1��K2�����Թܢ���װ���Լ�X��K1��K2��ͨ��CO2�������Ӻ������ǵ�ľ�������Թܢ��Һ���ϣ��۲쵽ľ������ȼ���Ң��еĵ���ɫû�б仯��
ʵ���ң���ʪ�Ķ�����̼�������Ƶķ�Ӧ
���Թܢ���װ���Լ�Y����������ͬʵ��ף��۲쵽ľ����ȼ���Ң��еĵ���ɫ��Ϊ��ɫ��
�Իش��������⣺
��1����װ��Na2O2��ͨ��CO2ǰ���ر�K1��K2��Ŀ����
��2����ʵ����У��Լ�X��
��3��������������ʵ�����õ��Ľ�����
��4����ʵ��������15.6g Na2O2�μӷ�Ӧ����ת�Ƶĵ�����Ϊ
��5��Ϊȷ����ʵ�������ȷ�ԣ��Ʊ�CO2���õķ�Ӧ�����ѡ��
A������ʯ�� B��С�մ� C���ռ D��ϡ���ᣮ
��������1����ֹ��Һ�е�ˮ�������������̼��
��2��X�Լ������Ǹ��������̼��Y�Լ������Ǹ�������̼�ṩˮ������
��3��ͨ��ʵ�����������
��4�����ݻ��ϼ۵ı仯����Ϲ������Ƶ���������ת�Ƶ��ӵ����ʵ�����
��5��С�մ���ϡ���ᷴӦ���ɶ�����̼��
��2��X�Լ������Ǹ��������̼��Y�Լ������Ǹ�������̼�ṩˮ������
��3��ͨ��ʵ�����������
��4�����ݻ��ϼ۵ı仯����Ϲ������Ƶ���������ת�Ƶ��ӵ����ʵ�����
��5��С�մ���ϡ���ᷴӦ���ɶ�����̼��
����⣺��1��Ϊ�˷�ֹ��Һ�е�ˮ�������������̼��������װ��Na2O2��ͨ��CO2ǰ���ر�K1��K2���ʴ�Ϊ����ֹCO2�ܳ���
��2��X�Լ������Ǹ��������̼������XΪŨ���Y�Լ������Ǹ�������̼�ṩˮ����������YΪCO2�ı�����Һ���ʴ�Ϊ��Ũ���CO2�ı�����Һ��
��3������Ķ�����̼ͨ���������ƣ�Ȼ�����ǵ�ľ�������Թܢ��Һ���ϣ��۲쵽ľ������ȼ���Ң��еĵ���ɫû�б仯��˵��û���������ɣ�������Ķ�����̼��������Ʋ���Ӧ�����Թܢ���װ���Լ�Y����������ͬʵ��ף��۲쵽ľ����ȼ���Ң��еĵ���ɫ��Ϊ��ɫ��˵������ˮ�����Ķ�����̼��������Ʒ�Ӧ���������ֻ̼����ˮ����ʱ���ܺ������Ʒ�Ӧ��
�ʴ�Ϊ��������ֻ̼����ˮ����ʱ���ܺ������Ʒ�Ӧ��
��4��2Na2O2+2CO2=2Na2CO3+O2��2e-��֪��2Na2O2����1molO2ʱ��ת�Ƶĵ�����Ϊ2mol����֪15.6g Na2O2�μӷ�Ӧ����n��Na2O2��=0.2mol������ת�Ƶ������ʵ���Ϊ0.2mol����ת�Ƶĵ�����Ϊ1.204��1023���ʴ�Ϊ��1.204��1023��
��5��С�մ���ϡ�������ɶ�����̼������ʯ��ϡ���ᷴӦ���ɵ�������������ʣ�����ѡ��С�մ���ϡ�����Ʊ�������̼���ʴ�Ϊ��B��D��
��2��X�Լ������Ǹ��������̼������XΪŨ���Y�Լ������Ǹ�������̼�ṩˮ����������YΪCO2�ı�����Һ���ʴ�Ϊ��Ũ���CO2�ı�����Һ��
��3������Ķ�����̼ͨ���������ƣ�Ȼ�����ǵ�ľ�������Թܢ��Һ���ϣ��۲쵽ľ������ȼ���Ң��еĵ���ɫû�б仯��˵��û���������ɣ�������Ķ�����̼��������Ʋ���Ӧ�����Թܢ���װ���Լ�Y����������ͬʵ��ף��۲쵽ľ����ȼ���Ң��еĵ���ɫ��Ϊ��ɫ��˵������ˮ�����Ķ�����̼��������Ʒ�Ӧ���������ֻ̼����ˮ����ʱ���ܺ������Ʒ�Ӧ��
�ʴ�Ϊ��������ֻ̼����ˮ����ʱ���ܺ������Ʒ�Ӧ��
��4��2Na2O2+2CO2=2Na2CO3+O2��2e-��֪��2Na2O2����1molO2ʱ��ת�Ƶĵ�����Ϊ2mol����֪15.6g Na2O2�μӷ�Ӧ����n��Na2O2��=0.2mol������ת�Ƶ������ʵ���Ϊ0.2mol����ת�Ƶĵ�����Ϊ1.204��1023���ʴ�Ϊ��1.204��1023��
��5��С�մ���ϡ�������ɶ�����̼������ʯ��ϡ���ᷴӦ���ɵ�������������ʣ�����ѡ��С�մ���ϡ�����Ʊ�������̼���ʴ�Ϊ��B��D��
���������⿼���˹��������������̼��Ӧ��̽��ʵ�飬�漰�Լ���ѡ�������ļ���ȣ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ