题目内容
【题目】已知短周期元素 A、B、C、D、E 的最高价氧化物对应的水化物分别为 X、Y、M、Z、W,B 是短周期主族元素中原子半径最大的元素,常温下 X、Y、Z、W 均可与 M 反应,A、B、D、E 的原子序数及其对应 0.1mol/L X、Y、Z 、W 溶液的 pH 如图所示。
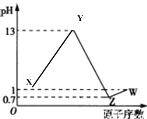
下列说法正确的是:
A. D的简单气态氢化物的热稳定性大于E的气态氢化物热稳定性
B. A、B、C 三种元素简单离子半径的大小顺序为C>B>A
C. Y 的稀溶液与 Z 或 W 的稀溶液分别发生中和反应时,对应的中和热在数值上相等
D. Y与W 两物质的化学键类型相同
【答案】C
【解析】
短周期元素A、B、C、D、E最高价氧化物对应水化物分别为X、Y、M、Z、W,B是短周期中原子半径最大的元素,则B为Na元素,则Y为NaOH;0.1mol/L的X、W溶液pH=1,则X和W均为一元强酸,且A的原子序数小于Na元素,E的原子序数大于Na元素,则A为N元素、X为HNO3;E为Cl元素、W为HClO4;0.1mol/L的Z溶液pH=0.7,则氢离子浓度为10-0.7mol/L=0.2mol/L,故Z为二元强酸,且D的原子序数大于Na元素,则D为S元素、Z为H2SO4;常温下X、Y、Z、W均可与M反应,则M为两性氢氧化物,则M为Al(OH)3、C为Al元素,据此解答。
短周期元素A、B、C、D、E最高价氧化物对应水化物分别为X、Y、M、Z、W,B是短周期中原子半径最大的元素,则B为Na元素,则Y为NaOH;0.1mol/L的X、W溶液pH=1,则X和W均为一元强酸,且A的原子序数小于Na元素,E的原子序数大于Na元素,则A为N元素、X为HNO3;E为Cl元素、W为HClO4;0.1mol/L的Z溶液pH=0.7,则氢离子浓度为10-0.7mol/L=0.2mol/L,故Z为二元强酸,且D的原子序数大于Na元素,则D为S元素、Z为H2SO4;常温下X、Y、Z、W均可与M反应,则M为两性氢氧化物,则M为Al(OH)3、C为Al元素,
A. 非金属性Cl>S,故氢化物稳定性HCl>H2S,故A错误;
B. N3-、Na+、Al3+电子层结构相同,核电荷数越大离子半径越小,故离子半径N3->Na+>Al3+,故B错误;
C. 中和热是指在稀溶液中,强酸跟强碱发生中和反应生成1 mol液态水时的反应热,所以NaOH的稀溶液与 HNO3或 HClO4的稀溶液分别发生中和反应时,对应的中和热在数值上相等,故C正确;
D. NaOH含有离子键、共价键,HClO4只含有共价键,二者含有化学键不全相同,故D错误。
答案选C。

【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
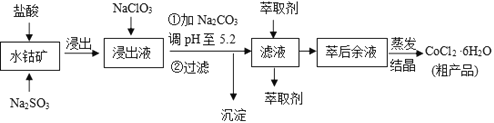
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式______________________________。
(2)写出NaClO3发生反应的主要离子方程式________________;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式_________________________________________________。
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为____________、_______________________
(4)制得的CoCl2·6H2O在烘干时需减压烘干的原因是__________________________。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是______。(答一条即可)
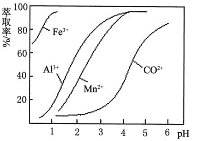
(6)萃取剂对金属离子的萃取率与pH的关系如图。萃取剂的作用是___________________;其使用的适宜pH范围是__________。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
【题目】工业上消除氮氧化物的污染,可用如下反应:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol
在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法不正确的是
A. 10 min内,T1时v(CH4)T2时小 B. 温度:T1<T2
C. ΔH:a < 0 D. 平衡常数:K(T1)<K(T2)


