题目内容
【题目】根据下面的元素周期表的图示,回答问题。
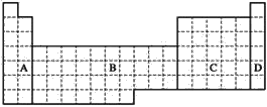
(1)全部是金属元素的区域为________。
(2)有人认为形成化合物最多的元素不是第ⅣA族的碳元素,而是另一种短周期元素。请你根据学过的化学知识判断,这一元素是________(写元素符号)。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置________。
②甲、乙两元素相比较,金属性较强的是________(填名称),可以验证该结论的实验是________。
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
【答案】B H 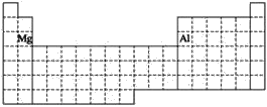 镁 bc
镁 bc
【解析】
(1)A区中H元素为非金属性,B区为过渡元素,全部为金属元素,C区中含有金属与非金属元素,D区为稀有气体,故答案为:B;
(2)有机物大都含有氢元素,非金属的氢化物中含有氢元素,H元素能与大多数的非金属元素形成化合物,形成化合物最多的元素可能是H元素,故答案为:H;
(3)甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,则甲为Al,乙元素原子核外M电子层与K电子层上的电子数相等,则乙为Mg;
①Al位于第三周期ⅢA族,Mg位于第三周期ⅡA族,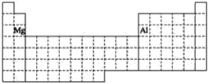 ;
;
②同周期自左而右元素金属性减弱,故金属性Mg>Al,则
a.金属在空气中放置已久,表面生成氧化物保护膜,阻止金属与水反应,不能比较金属性强弱,故错误;
b.将除掉表面氧化膜的这两种元素的单质分别和同浓度的盐酸反应,反应越剧烈,则元素金属性越强,故正确;
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液,比较碱性强弱,加入Mg粉的溶液呈浅红色,而加入Al粉的无明显现象,故正确;
d.二者都是金属元素,不能比较氢化物的稳定性判断金属性强弱,故错误;
综上bc正确。