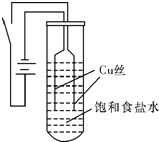
题目内容
【题目】实验室配制500mL0.5mol/L的NaCl溶液,有如下操作步骤:①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;②把①所得溶液小心转入500mL容量瓶中;③继续向容器瓶中加蒸馏水至液面距刻度1cm~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切;④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀.
(1)操作步骤的正确顺序为(填序号):
(2)本实验用到的基本仪器有:
(3)若出现如下情况,所配溶液浓度将偏高还是偏低:没有进行操作步骤④,会 ;加蒸馏水时不慎超过了刻度,会 ;定容时俯视会 。
(4)若实验过程中出现如下情况应如何处理?加蒸馏水时不慎超过了刻度,应 ;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面,应 。
【答案】
(1)① ② ③ ④ ⑤
(2)托盘天平、烧杯、玻璃棒、500 mL容量瓶、胶头滴管
(3)偏低 偏低 偏高
(4)倒掉重配 倒掉重配
【解析】
试题分析:(1)溶液的配制过程:计算—称量(量取)—溶解(稀释)—移液—洗涤—定容—摇匀—装瓶。因此其正确的步骤为①②③④⑤。
(2)所需的基本仪器可由实验步骤联想得出:托盘天平、烧杯、玻璃棒、500 mL容量瓶、胶头滴管。(3)对于误差的分析,应把握住基本的计算公式:![]() 。“没有洗涤烧杯、玻璃棒”,会使得溶质的量减少,从而导致浓度偏低。“加蒸馏水时不慎超过”,会使得体积变大,从而导致溶液浓度偏低。“定容时俯视”实际体积偏小,浓度变大。
。“没有洗涤烧杯、玻璃棒”,会使得溶质的量减少,从而导致浓度偏低。“加蒸馏水时不慎超过”,会使得体积变大,从而导致溶液浓度偏低。“定容时俯视”实际体积偏小,浓度变大。
(4)加蒸馏水时不慎超过了刻度,则溶液的体积无法确定,实验失败,要重新再配;转移液体时,不慎有液滴掉在容量瓶外面,则溶质的物质的量无法确定,实验失败,要重新再配;

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】碳元素是构成细胞的最基本元素,对此最有说服力的解释是 ( )
A. 碳在细胞的各种化合物中含量最多
B. 碳在自然界中含量最为丰富
C. 在细胞的各种化合物中都含有碳
D. 碳链构成了有机物的基本骨架
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r溶液为强酸溶液,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
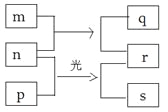
X | Y | |
Z | W |
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸