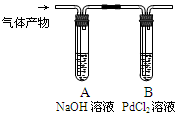
��Ŀ����
�������ӷ���ʽ������ȷ����
| A���⻯������Һ��ͨ������������Cl2+2Fe2+=2Fe3++2Cl�� |
| B����1mol/L 0.1L��������Һ�м���0.5mol/L 0.2L��Ba(OH)2��Һ�� 2Al3++3SO42��+ 3Ba2++6OH��=2Al(OH)3��+3BaSO4�� |
| C�������ǽ��ݵ������У�CO32��+2CH3COOH=2CH3COO��+ CO2��+H2O |
| D��������������ˮ��Ӧ��2O22��+2H2O=O2+4OH�� |
B
���������A�����ڻ�ԭ�ԣ�I-> Fe2+> Cl�������Ե⻯������Һ��ͨ������������������Ӧ��Cl2+2I-=I2+2Cl��.����B�������������ʵ����Ĺ�ϵ����дҲ�������ӷ���ʽ����дԭ����ȷ��C��������Ҫ�ɷֵ�CaCO3,������ˮ�������ǽ��ݵ������е����ӷ���ʽ�ǣ�CaCO3+ 2CH3COOH= Ca2++2CH3COO��+ CO2��+H2O������D�����������ǹ��壬����������ˮ��Ӧ�����ӷ���ʽ�ǣ�2Na2O2+2H2O=4Na++4OH��+O2��.����

��ϰ��ϵ�д�
 ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
�����Ŀ
 Cl2����H2����2OH��
Cl2����H2����2OH��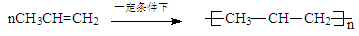

 K2S��N2����3CO2��
K2S��N2����3CO2��