题目内容
用a mol H2与b mol Cl2合成HCl,再将反应后的气体通入足量的NaOH溶液中充分吸收,按要求填写下表(可不填满):
①a="b " 无 2a或2b mol
②a>b 2(a-b) mol H2 2b mol
③a<b 无 (a+b) mol
27.(7分)在250 mL KI溶液中通入一定量的Cl2,再将所得溶液蒸干,并加热到质量不再减少为止,称得固体质量为23.2 g,经实验分析所得固体中含碘27.32%,试计算:
(1)原KI溶液的物质的量浓度。
(2)参加反应的Cl2有多少升(标准状况)?
| a和b大小关系 | 通过NaOH溶液后是否有气体剩余及其质量 | 生成NaCl物质的量 |
| | | |
| | | |
| | | |
| | | |
②a>b 2(a-b) mol H2 2b mol
③a<b 无 (a+b) mol
27.(7分)在250 mL KI溶液中通入一定量的Cl2,再将所得溶液蒸干,并加热到质量不再减少为止,称得固体质量为23.2 g,经实验分析所得固体中含碘27.32%,试计算:
(1)原KI溶液的物质的量浓度。
(2)参加反应的Cl2有多少升(标准状况)?
(1)c(KI)="1" mol·L-1
(2)V(Cl2)="2.24" L
(2)V(Cl2)="2.24" L
(1)23.2 g固体为KCl与KI,含碘为27.32%,则含KI为
27.32%×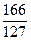 =35.7%
=35.7%
则m(KCl)="23.2" g×64.3%="14.9" g
参加反应的KI的物质的量为:
2KI + Cl2 ====2KCl+I2
2 mol 1mol 149 g
n′(KI)="0.2" mol 14.9 g
参加反应的Cl2为0.1 mol,标准状况下的体积为2.24 L
23.2 g固体中所含KI的质量为
23.2 g-14.9 g="8.3" g即0.05 mol
原KI溶液中的KI的物质的量浓度为:
c(KI)=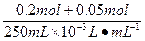 ="1" mol·L-1
="1" mol·L-1
(2)参加反应的Cl2在标准状况下的体积为2.24 L。
27.32%×
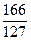 =35.7%
=35.7%则m(KCl)="23.2" g×64.3%="14.9" g
参加反应的KI的物质的量为:
2KI + Cl2 ====2KCl+I2
2 mol 1mol 149 g
n′(KI)="0.2" mol 14.9 g
参加反应的Cl2为0.1 mol,标准状况下的体积为2.24 L
23.2 g固体中所含KI的质量为
23.2 g-14.9 g="8.3" g即0.05 mol
原KI溶液中的KI的物质的量浓度为:
c(KI)=
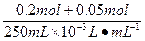 ="1" mol·L-1
="1" mol·L-1(2)参加反应的Cl2在标准状况下的体积为2.24 L。

练习册系列答案
相关题目
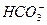 +OH-====CaCO3↓+H2O
+OH-====CaCO3↓+H2O