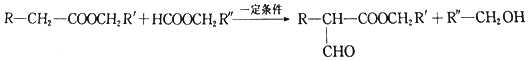
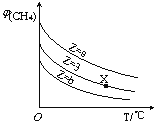
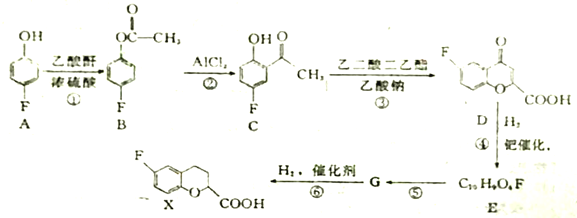
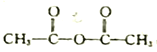
题目内容
【题目】钴、铁、镓、砷的单质及其化合物在生产生活中有重要的应用,请回答下列问题:
(1)写出砷(As)的基态原子的电子排布式_________。
(2)N、P、As为同一主族元素,其电负性从大到小的顺序为_______,它们的简单氢化物沸点最高的是______,将NaNO2和Na2O在一定的条件下反应得到一种白色晶体,已知其中的阴离子与SO42-互为等电子体,则该阴离子的化学式为________。
(3)Fe3+、Co3+、N3+-、CN-等可形成络合离子。
①K3Fe(CN)6]可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为________。
②[Co(N3)(NH3)5]SO4中Co的配位数为_______,其配离子中含有的化学健类型为_____(填离子键、共价键、配位键),C、N、O的第一电离能最大的是_____,其原因是_______。
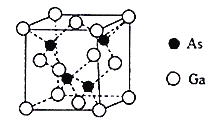
(4)砷化镓晶胞结构如图。晶跑中Ga与周围等距且最近的砷形成的空间构型为_____,已知砷化镓晶胞边长为apm,其密度为ρg·cm-3,则阿伏加德罗常数的数值为______(列出计算式即可)。
【答案】 [Ar] 3d104s24p3或1s22s22p63s23p63d104s24p3 N>P>As NH3 NO43- sp 6 共价键、配位键 N 氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子 正四面体 ![]()
【解析】(1)As的原子序数为33,由构造原理可知基态原子的电子排布式[Ar] 3d104s24p3;
(2)N、P、As为同一主族元素,其原子序数逐渐增大,则其电负性逐渐减小,即N>P>As ,它们的氢化物中NH3中存在氢键,沸点最高;原子个数相等价电子数相等的微粒属于等电子体,且等电子体结构相似,阴离子与SO42-互为等电子体,则该阴离子的化学式为NO43-。
(3)① CN-中碳原子价电子对个数=1+(4+1-1![]() 3)/2=2,所以采取sp杂化;
3)/2=2,所以采取sp杂化;
②[Co(N3)(NH3)5]SO4中N3-、NH3都是单齿配体,相加得配位数为6;其配离子中含有的化学健类型为共价键、配位键,C、N、O属于同一周期元素且原子序数依次增大,同一周期的第一电离能随原子序数增大而增大,但氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子,所以第一电离能最大的是N 。
(4)晶跑中Ga原子处于晶体的顶点和面心,面心到顶点和到相邻面心的距离最小且相等,Ga原子与周围等距且最近的砷形成的空间构型为Ga在中心,As在四个顶点形成的正四面体结构;GaAs为1:1型结构,一个晶胞含有4个Ga原子和4个As原子,若晶胞边长为apm,则其体积为(a![]() 10-10)3cm3,晶胞密度为ρg·cm-3,则晶胞质量为(a
10-10)3cm3,晶胞密度为ρg·cm-3,则晶胞质量为(a![]() 10-10)3cm3
10-10)3cm3![]() ρg·cm-3=ρa3
ρg·cm-3=ρa3![]() 10-30g, ρa3
10-30g, ρa3![]() 10-30g
10-30g![]() NA=4
NA=4![]() 145g/mol,则为
145g/mol,则为![]() 。
。

【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.76mol/L
B.830℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4
【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
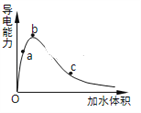
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。
(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。