题目内容
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.NH3 ![]() NO
NO ![]() NaNO2
NaNO2
B.Fe2O3 ![]() Fe
Fe ![]() FeCl3
FeCl3
C.SiO2 ![]() H2SiO3(aq)
H2SiO3(aq) ![]() Na2SiO3
Na2SiO3
D.CuCl2(aq) ![]() Cu(OH)2
Cu(OH)2 ![]() Cu2O
Cu2O
【答案】B
【解析】解:A.氨气与氧气反应生成NO,NO与氢氧化钠不反应,不能转化为亚硝酸钠,所以不能实现转化,故A错误;
B.Fe2O3与Al粉混合物发生铝热反应,实质是置换反应,生成铁和氧化铝,方程式为:2Al+Fe2O3 ![]() 2Fe+Al2O3 , 氯气能将金属氧化为最高价,铁在氯气中燃烧的产物是氯化铁,反应为:2Fe+3Cl2
2Fe+Al2O3 , 氯气能将金属氧化为最高价,铁在氯气中燃烧的产物是氯化铁,反应为:2Fe+3Cl2 ![]() 2FeCl3 , 能实现转化,故B正确;
2FeCl3 , 能实现转化,故B正确;
C.二氧化硅不溶于水,二氧化硅与水不反应,无法一步得到硅酸,故C错误;
D.氯化铜和氢氧化钠反应生成氢氧化铜,CuCl2+2NaOH=Cu(OH)2↓+2NaCl,氢氧化铜和葡萄糖加热反应生成氧化亚铜红色沉淀,C6H12O6+2Cu(OH)2 ![]() CH2(OH)(CHOH)4COOH+Cu2O↓+2H2O,氢氧化铜和蔗糖不反应,所以不能实现转化,故D错误;
CH2(OH)(CHOH)4COOH+Cu2O↓+2H2O,氢氧化铜和蔗糖不反应,所以不能实现转化,故D错误;
故选B.
A.NO与氢氧化钠不反应;
B.铝的金属性强于铁,铝和氧化铁发生铝热反应,氯气具有强氧化性,具有变价的铁与氯气反应生成氯化铁;
C.二氧化硅不溶于水;
D.氯化铜和氢氧化钠反应生成氢氧化铜,但氢氧化铜和蔗糖不反应,不能生成氧化亚铜红色沉淀.

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】实验室用环己醇脱水的方法合成环己烯,该实验的装置如下图所示:
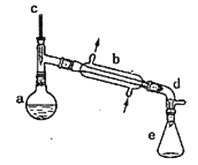
可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是________;b的名称是________;
(2)a中发生主要反应的化学方程式为____________________________;本实验最容易产生的有机副产物的结构简式为________。
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加人无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是________,操作X的名称为________。
Ⅲ.产物分析及产率计算
(4)①核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有_______种不同化学环境的氢原子。
② 本实验所得环己烯的产率是_______。