题目内容
(4分)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化成液态水时放热2.444KJ,试写出氢气的燃烧热的热化学方程式——————————————————————————————————————。
H2(g)+1/2O2(g)=H2O(l) △H="-285.8KJ" ?mol-1
燃烧热是指在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,1mol水蒸气变成液态水又放出热量是2.444KJ×2=4.888KJ,所以氢气的燃烧热是241.8KJ/mol+4.888KJ/mol=285.8KJ /mol,所以热化学方程式为H2(g)+1/2O2(g)=H2O(l) △H=-285.8KJ ?mol-1。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目


 C、
C、 分别按下式反应(燃烧):
分别按下式反应(燃烧): 放热
放热
 放热
放热
 放热
放热

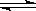 SO3(g) △H = -98.32kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
SO3(g) △H = -98.32kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为