题目内容
【题目】下图中的每一个方格表示有关的一种反应物或生成物,其中X为正盐,A、C、D均为无色气体,且气体C的水溶液显碱性。
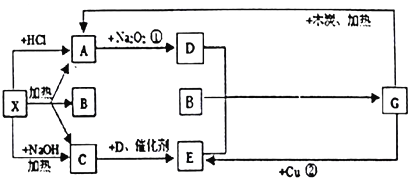
(1)用化学用语按要求填空:
X的化学式为:__________,X中含有化学键类型为__________;A的电子式__________。
(2)写出反应②的离子方程式___________________________。
(3)过量的Fe粉与G的稀溶液反应,向反应后溶液中加入碱溶液,现象是________________。
【答案】 ![]() 离子键、共价键
离子键、共价键 ![]()
![]() 先产生白色沉淀,随后变为灰绿色,最后生成红褐色沉淀
先产生白色沉淀,随后变为灰绿色,最后生成红褐色沉淀
【解析】X和NaOH反应生成无色气体C,推知C为NH3,X是铵盐;X和盐酸反应生成无色气体A,A和Na2O2反应生成D,推知A为CO2,D为O2,进而推出E为NO,F为NO2,G为HNO3,浓度不同时,能和铜反应生成不同的气体,则X可能是
NH4HCO3或 (NH4)2 CO3,其中![]() 为正盐,为(NH4)2 CO3,则
为正盐,为(NH4)2 CO3,则
(1)X的化学式为:(NH4)2 CO3,NH4+ 与CO32―之间形成离子键,C―O,N―H形成共价键;A的电子式![]() ;(2)写出反应②的离子方程式铜与浓硝酸反应生成NO2,Cu+4H++2NO3―=Cu2++2NO2↑+4H2O;(3)过量铁粉和稀硝酸反应生成硝酸亚铁,向反应后溶液中加入碱溶液,现象是①有白色絮状沉淀生成,但很变灰绿色,最变成红褐色(原因:生成的氢氧化亚铁迅速被空气中的氧氧化变为氢氧化铁) ②有红褐色沉淀 化学方程式:Fe2++2OH-=Fe(OH)2↓, 4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,Fe3++3OH-=Fe(OH)3↓。
;(2)写出反应②的离子方程式铜与浓硝酸反应生成NO2,Cu+4H++2NO3―=Cu2++2NO2↑+4H2O;(3)过量铁粉和稀硝酸反应生成硝酸亚铁,向反应后溶液中加入碱溶液,现象是①有白色絮状沉淀生成,但很变灰绿色,最变成红褐色(原因:生成的氢氧化亚铁迅速被空气中的氧氧化变为氢氧化铁) ②有红褐色沉淀 化学方程式:Fe2++2OH-=Fe(OH)2↓, 4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,Fe3++3OH-=Fe(OH)3↓。

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目