题目内容
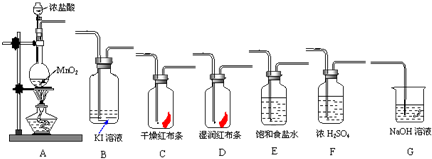
实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:
MnO2+4HCl(浓)![]() Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
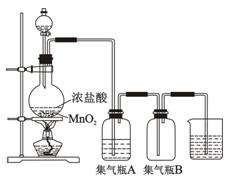
试回答下列问题:
(1)该反应是氧化还原反应吗?① (填“是”或“不是”),如果是氧化还原反应,指出②氧化剂是 ,③还原剂是 ,④写出该反应的离子方程式 。
(2)集气瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯
化氢在饱和食盐水中的溶解度则很大),其作用是 。
(3)氯气溶于水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中
毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用 溶液来吸收有毒的氯气。
(4)一次实验中,加入浓盐酸200mL,其密度为1.19g·cm-3、HCl的质量分数为36.5%,
当MnO2刚好完全反应时,产生了5.6L(标准状况)的氯气。
试计算该浓盐酸的物质的量浓度和被氧化的HCl的物质的量。(请写出计算过程)
(1)① 是;② MnO2;③ 浓盐酸;
④ 4H++2Cl-+MnO2![]() Cl2↑+Mn2++2H2O;
Cl2↑+Mn2++2H2O;
(2)除去氯气中混有的HCl气体 (3)浓氢氧化钠(浓碱)
(4)(计算过程略)浓盐酸的物质的量浓度是:11.9 mol/L
被氧化的HCl的物质的量为: 0.5mol
解析:
略

练习册系列答案
相关题目