题目内容
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是( )
A. 1mol甲烷完全燃烧转移的电子数为8NA
B. 18g的D2O中含有的质子数为10NA
C. 28g的乙烯和环己烷混合气体中所含原子总数为6NA
D. 1L1mol/L的NH4C1溶液中NH4+和Cl—的数目均为NA
【答案】AC
【解析】
A、CH4中C的化合价为-4价,甲烷燃烧后生成CO2,因此1mol甲烷燃烧后,转移电子物质的量为1mol×[4-(-4)]=8mol,故A正确;
B、D2O的摩尔质量为20g·mol-1,即18gD2O中含有质子的物质的量为![]() =9mol,故B错误;
=9mol,故B错误;
C、乙烯分子式为C2H4,环己烷分子式为C6H12,通式为CnH2n,含有原子的物质的量为![]() 6mol,故C正确;
6mol,故C正确;
D、NH4Cl属于强酸弱碱盐,NH4+水解,即NH4+的物质的量应小于1L×1mol·L-1=1mol,故D错误;
答案为AC。

 字词句篇与同步作文达标系列答案
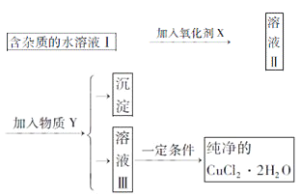
字词句篇与同步作文达标系列答案【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性,将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH的数据如下表所示。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
氢氧化物 | 开始沉淀pH | 完全沉淀pH |
Fe(OH)2 | 6.5 | 9.7 |
Fe(OH)3 | 1.5 | 3.7 |
Cu(OH)2 | 4.2 | 6.7 |
请回答下列问题:
(1)本实验最适合的氧化剂X是__________。(选填下面的序号)
A K2Cr2O7 B NaClO C H2O2 D KMnO4
(2)物质Y是________。
(3)本实验用加碱沉淀的目的是否能达到?________________。原因是________________。
(4)除去Fe3+的化学方程式为____________________,_________________________________。
(5)加氧化剂的目的为________________________。
(6)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________________。应如何操作________________。