题目内容
1.无水氯化铝是白色晶体,易吸收水分,在178℃升华.装有无水氯化铝的试剂瓶久置于潮湿空气中,会爆炸并产生大量白雾,氯化铝常作为石油化工的催化剂,并用于处理润滑剂等.某课外兴趣小组在实验室里,通过如图所示装置制取少量纯净的无水氯化铝.
(1)B、C中盛放的试剂分别为饱和食盐水 浓硫酸(填试剂名称)
(2)在E处可收集到纯净的氯化铝,其原因是氯化铝在178℃升华,氯化铝受热升华,在E处凝结.
(3)从A装置导出的气体若不经过B、C装置而直接进入D中玻璃管,将对实验产生的后果是未经除去的氯化氢和水蒸气随氯气进入D中和铝能反应生成氢气,氢气和氯气混合会发生爆炸.
(4)F装置所起的作用是吸收多余的氯气,防止污染环境;防止空气中的水蒸气进入D中.
分析 (1)氯化氢易挥发,制取的氯气中含有氯化氢和水,进入装置D前应除去,依据氯化氢、浓硫酸的性质选择合适的试剂;
(2)氯化铝易升华,生成的氯化铝气体会聚集在E处;
(3)根据混合气体的成分和性质判断;
(4)氯气有毒,污染环境,所以不能排空;碱石灰的成分是氧化钙和氢氧化钠,氯气和氧化钙、氢氧化钠能反应达到,所以可用碱石灰处理尾气;空气中有水蒸气,碱石灰还能吸收水蒸气,所以可作干燥剂.
解答 解:(1)浓盐酸具有挥发性,所以混合气体中含有氯化氢;氯化氢极易溶于水,氯气在饱和食盐水中溶解度不大,可以选择饱和食盐水吸收氯化氢,浓硫酸具有吸水性,能够干燥氯气;
故答案为:饱和食盐水,浓硫酸;
(2)氯化铝在178℃升华,产物以气体形式存在,主要聚集在C处,故可以在E收集;
故答案为:氯化铝在178℃升华,产物以气体形式存在,主要聚集在C处;
(3)因浓盐酸具有挥发性.反应生成物中有水,在加热条件下变成水蒸汽,所以混合气体中的成分是氯化氢、水蒸气、氯气;氯化氢和铝能反应生成氢气,氢气和氯气混合会发生爆炸;
故答案为:未经除去的氯化氢和水蒸气随氯气进入D中和铝能反应生成氢气,氢气和氯气混合会发生爆炸;(4)氯气有毒,污染环境,所以不能排空;碱石灰的成分是氧化钙和氢氧化钠,氯气和氧化钙、氢氧化钠能反应达到,所以可用碱石灰处理尾气;空气中有水蒸气,碱石灰还能吸收水蒸气,所以可作干燥剂防止空气中的水蒸气进入D中;
故答案为:吸收多余的氯气,防止污染环境;防止空气中的水蒸气进入D中.
点评 本题通过氯化铝的制取,考查了氯气的制备和性质的检验,熟悉反应原理是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列气体中,极易溶于水的是( )
| A. | Cl2 | B. | NH3 | C. | C2H4 | D. | C2H6 |
1.下列物质的制取原理错误的是( )
| A. | 金属钠的制取:2NaCl(熔融)$\stackrel{通直流电}{→}$2Na+C12↑ | |
| B. | 金属镁的制取:MgO+CO$\stackrel{加热}{→}$Mg+CO2 | |
| C. | 金属铬的制取:Cr2O3+2Al$\stackrel{高温}{→}$2Cr+Al2O3 | |
| D. | 金属汞的制取:2HgO$\stackrel{加热}{→}$2Hg+O2↑ |
13.如图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( )
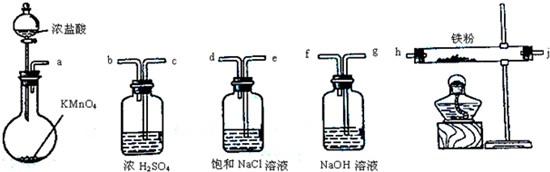

| A. | a-b-c-d-e-e-f-g-h | B. | a-e-d-c-b-h-j-g | ||
| C. | a-d-e-c-b-h-j-g | D. | a-c-b-d-e-h-j-f |
10.某同学做元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验内容:(填写与实验步骤对应的实验现象的编号和②③的化学方程式)
(2)填写编号③④⑤的化学方程式
实验③2Na+2H2O=2NaOH+H2↑
实验④Mg+2HCl=MgCl2+H2↑,
实验⑤2Al+6HCl=2AlCl3+3H2↑;
(2)实验结论:同周期从左至右元素金属性减弱,非金属性增强.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
(1)实验内容:(填写与实验步骤对应的实验现象的编号和②③的化学方程式)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
实验③2Na+2H2O=2NaOH+H2↑
实验④Mg+2HCl=MgCl2+H2↑,
实验⑤2Al+6HCl=2AlCl3+3H2↑;
(2)实验结论:同周期从左至右元素金属性减弱,非金属性增强.
11.下列有关化工生产的说法中,不正确的是( )
| A. | 工业上用热还原法冶炼铁:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe | |
| B. | 硫酸工业、合成氨工业和氯碱工业均采用了循环操作提高原料的利用率 | |
| C. | 利用反应:NaCl(饱和)+CO2+NH3+H2O=NaHCO3↓+NH4Cl制取NaHCO3时,应先通入过量的NH3,再通入过量的CO2 | |
| D. | 硫酸生产中常采用高压条件提高SO2的转化率 |