题目内容
在一真空容器中,充入10 mol N2,30 mol H2,发生反应N2(g)+3H2(g) 2NH3(g),在一定条件下达到平衡时,N2的转化率为25%。若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )
2NH3(g),在一定条件下达到平衡时,N2的转化率为25%。若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )
 2NH3(g),在一定条件下达到平衡时,N2的转化率为25%。若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )
2NH3(g),在一定条件下达到平衡时,N2的转化率为25%。若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )| A.20 mol、25% | B.20 mol、75% | C.40 mol、30% | D.10mol、50% |
B
据合成氨气的化学方程式知,10 mol N2和30 mol H2反应,当N2的转化率为25%时,有2.5 mol N2参加反应生成5 mol NH3。同时,据化学反应的可逆性,10 mol N2与30 mol H2混合作为起始条件相当于20 mol NH3作为起始条件,此情况下当只剩5 mol NH3时,有15 mol NH3已转化为N2、H2,此时NH3的转化率为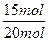 ×100%=75%,所以选B。
×100%=75%,所以选B。
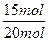 ×100%=75%,所以选B。
×100%=75%,所以选B。
练习册系列答案
相关题目
 cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )
cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是( )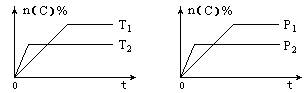
 N2O3(g)+O2(g),②N2O3(g)
N2O3(g)+O2(g),②N2O3(g) 2H2(g)+O2 (g)
2H2(g)+O2 (g) 2R(g)+W(g),反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为( )
2R(g)+W(g),反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为( ) 2HI(g)达到平衡的标志是( )
2HI(g)达到平衡的标志是( ) N2O4。平衡时测得NO2的转化率为a%。其他条件不变,再充入1 mol NO2,待新平衡建立时,测得NO2的转化率为b%。则a和b的大小关系为________________。
N2O4。平衡时测得NO2的转化率为a%。其他条件不变,再充入1 mol NO2,待新平衡建立时,测得NO2的转化率为b%。则a和b的大小关系为________________。