题目内容
(本题共6分)盐酸、硫酸和硝酸是三种重要的酸。
(1)工业上生产盐酸与硝酸时,都要用到的气态物质是 ;
(2)工业上生产硫酸与硝酸时,用到的相同的重要设备是 ;
(3)工业上生产的盐酸与硝酸有可能呈黄色,请用化学方程式表示硝酸溶液呈黄色的原 因 ;
(4)浓硫酸与浓硝酸都可用铁、铝容器贮存的相同原理是 ;
(5)浓盐酸与浓硝酸暴露在空气中,相同的现象是 。
(本题共6分,每个问题均1分)
(1)H2 ;(2)吸收塔;(3)
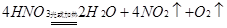 ;
;
(4) 铁、铝被浓硝酸或浓硫酸钝化;(5)产生白雾;(6)SO2
【解析】
试题分析:(1)工业上生产盐酸需要氢气和氯化氢,制取硝酸需要的是氢气和氮气,所以,都要用到的气态物质是氢气。
(2)工业上生产硫酸与硝酸时,用到的相同的重要设备是吸收塔。
(3)由于浓硝酸易分解生成NO2,NO2溶解在浓硝酸中而显黄色,方程式是4HNO3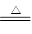 2H2O+4NO2↑+O2↑。
2H2O+4NO2↑+O2↑。
(4)在常温下,铁或铝在浓硫酸或浓硝酸中都发生钝化,所以浓硫酸与浓硝酸都可用铁、铝容器贮存。
(5)浓硝酸和浓盐酸都极易挥发性,所以浓盐酸与浓硝酸暴露在空气中,相同的现象是产生白雾。
考点:考查硝酸、盐酸和硫酸的性质、制取、储存等
点评:三种物质虽然都是强酸,但硝酸和浓硫酸还是氧化性酸,都具有强氧化性。

(本题共6分)
某学生课外兴趣小组为了测定镁铝合金中铝的含量,进行了如下实验。将合金3.0克投入到足量的100 mL 1.5 mol?L-1的烧碱溶液中,充分反应后分离出未反应的镁,然后在溶液中滴加1.0 mol?L-1的盐酸,加入盐酸的体积与得到沉淀的数据如下表:
| 实验次数 | 加入盐酸的体积 | 沉淀质量 |
| 1 | 60 mL | 0 |
| 2 | 80 mL | 0.78 g |
| 3 | 180 mL | 5.46 g |
(2)合金中铝的质量分数为 。
实验题:(本题共9分)某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:?
| A.在250 mL的容量瓶中配制250 mL烧碱溶液; | B.用碱式滴定管量取25.00 mL烧碱溶液于锥形瓶中并滴加几滴酚酞做指示剂;? | C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解; | D.将物质的量浓度为cmol/L的标准盐酸溶液装入酸式滴定管。调整液面记下开始读数为V1 mL;E.在锥形瓶下垫一张白纸,滴定最后一滴至红色刚好消失 为止,半分钟后不恢复红色,记下读数V2 mL。? 为止,半分钟后不恢复红色,记下读数V2 mL。? |
(1)正确操作步骤的顺序是:(用编号字母填写) ?。
(
 2)观察滴定管里液面的高度时应注意: 。?
2)观察滴定管里液面的高度时应注意: 。?(3)E步骤的操作中在锥形瓶下垫一张白纸的作用是 。
(4)D步骤的操作中液面应调节到 ,尖嘴部分应 。
(5)某学生实验时把锥形瓶用烧碱样品洗涤,使测定的浓度偏高还是偏低?
(6)该烧碱样品纯度的计算式为:
(本题共6分)
某学生课外兴趣小组为了测定镁铝合金中铝的含量,进行了如下实验。将合金3.0克投入到足量的100 mL 1.5 mol•L-1的烧碱溶液中,充分反应后分离出未反应的镁,然后在溶液中滴加1.0 mol•L-1的盐酸,加入盐酸的体积与得到沉淀的数据如下表:
|
实验次数 |
加入盐酸的体积 |
沉淀质量 |
|
1 |
60 mL |
0 |
|
2 |
80 mL |
0.78 g |
|
3 |
180 mL |
5.46 g |
(1)开始沉淀时加入的盐酸体积必须大于 mL;若得到沉淀的量最大时,加入的盐酸体积为 mL。
(2)合金中铝的质量分数为 。