题目内容
【题目】两种气态烃组成的混合气体0.1 mol,完全燃烧得0.16 mol CO2和3.6 g H2O,下列说法正确的是
A. 混合气体中一定有甲烷 B. 混合气体一定是甲烷和乙烯
C. 混合气体中可能有乙炔 D. 混合气体中一定有乙炔
【答案】A
【解析】水的物质的量是3.6g÷18g/mol=0.2mol,则根据原子守恒可知该混合烃平均分子组成为C1.6H4,故两种烃中一种分子所含碳原子数大于1.6,另一种小于1.6,而分子中所含碳原子数小于1.6的烃只有CH4,故混合气体中一定含CH4,则另一种烃分子中必含4个H,可能为C2H4、C3H4等,A正确,B、C、D错误,答案选A。

【题目】现有一瓶A和B的混合物,已知甲和乙的某些性质如表所示:( )
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 水中的溶解性 |
A | -75 | 66 | 0.93 | 可溶 |
B | -66 | 110 | 0.90 | 可溶 |
据此,将甲和乙互相分离的方法是( )
A.蒸馏法B.升华法C.萃取法D.过滤法
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:① 2Fe3++H2O2 == 2Fe2++O2↑+2H+,② H2O2+2Fe2++2H+ == 2H2O+2Fe3+。反应过程中能量变化如下图所示。下列说法错误的是
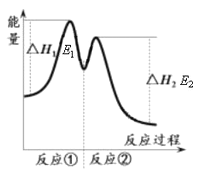
A. Fe3+的作用是增大过氧化氢的分解速率
B. 反应①是吸热反应、反应②是放热反应
C. 反应2H2O2(aq) == 2H2O(l)+O2(g)的ΔH=E1-E2<0
D. 0~6 min的平均反应速率:v(H2O2)=3.33×10-2 mol·L-1·min-1



