题目内容
【题目】化合物M可用于消毒剂、抗氧化剂、医药中间体。实验室由芳香烃A制备M的一种合成路线如下:

请回答:
(1)B的化学名称为___________;D中官能团的名称为______________________。
(2)由F生成G的反应类型为___________;F的分子式为___________。
(3)由E转化为F的第一步反应的化学方程式为______________________。
(4)M的结构简式为___________。
(5)芳香化合物Q为C的同分异构体,Q能发生银镜反应,其核磁共振氢谱有4组吸收峰。写出符合要求的Q的一种结构简式______________________。
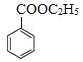
(6)参照上述合成路线和信息,以苯甲酸乙酯和CH3MgBr为原料(无机试剂任选),设计制备 的合成路线_________________________________。
的合成路线_________________________________。
【答案】对甲基苯甲醛(或4﹣甲基苯甲醛) 羧基、氯原子 酯化反应或取代反应 C8H12O2 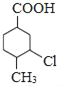 +2NaOH
+2NaOH![]()
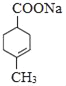 +NaCl+2H2O
+NaCl+2H2O 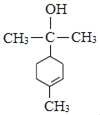
![]() 或
或![]() ;
; 
![]()
![]()
![]()
【解析】
A的分子式为C7H8,结合B的结构,应是A与CO发生加成反应生成B(对甲基苯甲醛),可知A为![]() 。对比B与C的结构,结合反应条件、C的分子式,可知B中醛基氧化为羧基得到C,C与氯气发生苯环上取代反应生成D,D与氢气发生加成反应生成E,E发生取代反应生成F,故C为
。对比B与C的结构,结合反应条件、C的分子式,可知B中醛基氧化为羧基得到C,C与氯气发生苯环上取代反应生成D,D与氢气发生加成反应生成E,E发生取代反应生成F,故C为![]() 、D为
、D为![]() 、E为
、E为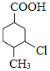 。F与乙醇发生酯化反应生成G为
。F与乙醇发生酯化反应生成G为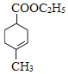 ,G发生信息中反应生成M为
,G发生信息中反应生成M为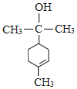 ,据此分析解答。
,据此分析解答。
(1)B的结构简式为![]() ,名称为对甲基苯甲醛(或4﹣甲基苯甲醛);D为
,名称为对甲基苯甲醛(或4﹣甲基苯甲醛);D为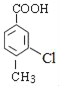 ,其中 官能团有羧基、氯原子,故答案为:对甲基苯甲醛(或4﹣甲基苯甲醛);羧基、氯原子;
,其中 官能团有羧基、氯原子,故答案为:对甲基苯甲醛(或4﹣甲基苯甲醛);羧基、氯原子;
(2)由F生成G发生酯化反应,也属于取代反应;F的分子式为C8H12O2,故答案为:酯化反应或取代反应;C8H12O2;
(3)由E转化为/span>F的第一步反应的化学方程式为: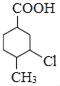 +2NaOH
+2NaOH![]()
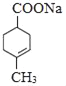 +NaCl+2H2O,故答案为:
+NaCl+2H2O,故答案为: +2NaOH
+2NaOH![]()
 +NaCl+2H2O;
+NaCl+2H2O;
(4)由分析可知M的结构简式为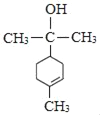 ,故答案为:
,故答案为: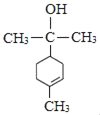 ;
;
(5)芳香化合物Q为C(![]() )的同分异构体,Q能发生银镜反应,说明含有醛基或甲酸形成的酯基,其核磁共振氢谱有4组吸收峰。符合要求的Q的结构简式为:
)的同分异构体,Q能发生银镜反应,说明含有醛基或甲酸形成的酯基,其核磁共振氢谱有4组吸收峰。符合要求的Q的结构简式为:![]() 、
、![]() ,故答案为:
,故答案为:![]() 或
或![]() ;
;
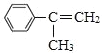
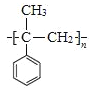
(6) 加聚反应得到
加聚反应得到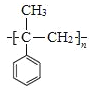 ,
,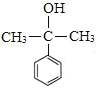 发生消去反应得到
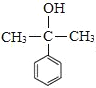
发生消去反应得到 ,由信息可知苯甲酸乙酯与①CH3MgBr、②H+/H2O作用得到
,由信息可知苯甲酸乙酯与①CH3MgBr、②H+/H2O作用得到 ,合成路线流程图为
,合成路线流程图为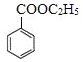
![]()

![]()

![]()
 ,故答案为:
,故答案为:
![]()

![]()

![]()
 。
。



