题目内容
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。
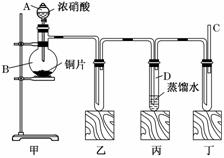
请回答下列问题:
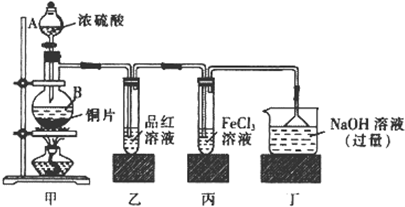
(1)装置甲中盛放浓硝酸的仪器A的名称是________,该装置中发生反应的化学方程式为_______________________。
(2)实验过程中,装置乙、丙中出现的现象分别是:
_____________________________、___________________________;
装置丙中的试管内发生反应的离子方程式为:____________________。
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是________________________________________。
(4)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________色,为了证明铁元素在该反应中的产物,可以再在溶液中滴加KSCN溶液,溶液变为________色。有关方程式___________________________、
______________________________________;
(1)分液漏斗
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O(2分)
(2)生成红棕色气体 蒸馏水中有气泡产生,生成无色气体 3NO2+H2O===2H++2NO![]() +NO(2分)
+NO(2分)
(3)氧气
(4)黄 红(或“血红”)4H++NO3-+3Fe2+=NO+H2O+3Fe3+(2分),Fe3++3SCN=Fe(SCN)3(2分)其余每空1分

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目