题目内容
 (1)铜板上铁铆钉处容易生锈,称为
(1)铜板上铁铆钉处容易生锈,称为电化学(或吸氧)
电化学(或吸氧)
腐蚀,被腐蚀的金属是铁
铁
;原电池的正极电极反应式是O2 +4e-+2H2O═4OH-
O2 +4e-+2H2O═4OH-
.(2)如图所示的铜-锌原电池中,理论上应观察到的现象是:铜片上
有气泡产生
有气泡产生
,此时原电池的负极电极反应式是Zn-2e-═Zn2+
Zn-2e-═Zn2+
.分析:(1)金属在潮湿的空气中易发生吸氧腐蚀,在原电池的正极是氧气得电子的过程;
(2)在原电池中,活泼金属做负极,发生失电子的氧化反应,正极上是电解质中的阳离子发生得电子得还原反应.
(2)在原电池中,活泼金属做负极,发生失电子的氧化反应,正极上是电解质中的阳离子发生得电子得还原反应.
解答:解:(1)铜板上铁铆钉处容易生锈,是因为金属铁、铜、潮湿的空气形成了原电池,其中活泼金属铁发生了吸氧腐蚀的结果,在该原电池的正极上是氧气得电子的过程,
故答案为:电化学(或吸氧);铁;O2+4e-+2H2O═4OH-;
(2)在铜、锌、硫酸原电池中,活泼金属锌做负极,发生失电子的氧化反应,即Zn-2e-═Zn2+,金属铜作正极,正极上是氢离子发生得电子得还原反应,即2H++2e-→H2↑,有气泡产生,
故答案为:有气泡产生;Zn-2e-═Zn2+.
故答案为:电化学(或吸氧);铁;O2+4e-+2H2O═4OH-;
(2)在铜、锌、硫酸原电池中,活泼金属锌做负极,发生失电子的氧化反应,即Zn-2e-═Zn2+,金属铜作正极,正极上是氢离子发生得电子得还原反应,即2H++2e-→H2↑,有气泡产生,
故答案为:有气泡产生;Zn-2e-═Zn2+.
点评:本题考查学生原电池的工作原理知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目




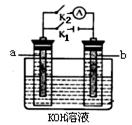
 (2)图2中a、b是多孔石墨电极,断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,b极上的电极反应式为 ,OH-向 (填a或b)极移动。然后断开K1,闭合K2,观察到电流计A的指针有偏转。b极上的电极反应式为 ,OH-向 (填a或b)极移动。
(2)图2中a、b是多孔石墨电极,断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,b极上的电极反应式为 ,OH-向 (填a或b)极移动。然后断开K1,闭合K2,观察到电流计A的指针有偏转。b极上的电极反应式为 ,OH-向 (填a或b)极移动。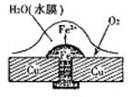
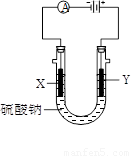
 (2)图2中a、b是多孔石墨电极,断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,b极上的电极反应式为
,OH-向
(填a或b)极移动。然后断开K1,闭合K2,观察到电流计A的指针有偏转。b极上的电极反应式为
,OH-向 (填a或b)极移动。
(2)图2中a、b是多孔石墨电极,断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,b极上的电极反应式为
,OH-向
(填a或b)极移动。然后断开K1,闭合K2,观察到电流计A的指针有偏转。b极上的电极反应式为
,OH-向 (填a或b)极移动。