题目内容
高炉炼铁过程中发生的主要反应为1/3Fe2O3(s) + CO(g) 2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min达到平衡。求该时间范围内反应的平均反应速率υ(CO2)=" _________" 、CO的平衡转化率= _____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
| A.减少Fe的量 |
| B.增加Fe203的量 |
| C.移出部分CO2 |
| D.提高反应温度 |
F.加入合适的催化剂
⑴ K=c(CO2)/c(CO) < ⑵ 0.006mol/(L·min) 60℅ ⑶ C
解析试题分析:(1)根据化学平衡常数的定义可知:K=c(CO2)/c(CO)。由于温度升高化学平衡常数。说明升高温度,平衡向逆反应方向移动。逆反应是吸热反应,该反应的正反应为放热反应 △H<0;
(2) 1/3Fe2O3(s) + CO(g)  2/3Fe(s) + CO2(g)
2/3Fe(s) + CO2(g)
起: 1 mol 1 mol 1 mol 1 mol
变: 1/3x x 2/3x x
终: 1 mol- 1/3x 1 mol- x 1 mol+ 2/3x 1 mol+ x
平衡常数只与温度有关,且已知1000℃时 K=4.0
即:K=c(CO2)/c(CO)=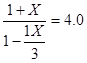 解得:x = 0.6 mol 则υ(CO2)= 0.6 mol/ (10L·l0 min) = 0.006 mol/ (L·min)
解得:x = 0.6 mol 则υ(CO2)= 0.6 mol/ (10L·l0 min) = 0.006 mol/ (L·min)
CO的平衡转化率= 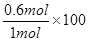 ℅ = 60℅
℅ = 60℅
(3)因Fe和Fe2O3为固体,对平衡没有影响所以A、B错误;C中CO2为气体生成物,减少生成物浓度平衡向正反应方向移动,故C正确;升高温度平衡向吸热反应方向移动。对于该反应来说是向逆反应方向移动,CO的平衡转化率降低。D错误;因为该反应是前后气体相等的可逆反应。所以减小容器的容积也就是增大压强。化学平衡不发生移动。CO的平衡转化率不变。E错误;催化剂只改变化学反应速率而不影响平衡的移动,故F错误。
考点:考查化学平衡常数、化学反应速率的计算及外界条件对反应物的转化率的影响的知识。

 阅读快车系列答案
阅读快车系列答案利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。
已知:SO2(g)+ O2(g)
O2(g) SO3(g) △H=-98 kJ·mol-1。
SO3(g) △H=-98 kJ·mol-1。
(1)某温度下该反应的平衡常数K=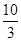 ,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”)。
,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”)。
(2)一定温度下,向一带活塞的体积为2 L的密闭容器中充入2.0 mol SO2和1.0 molO2,达到平衡后体积变为1.6 L,则SO2的平衡转化率为 。
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母)。
| A.保持温度和容器体积不变,充入1.0 mol O2 |
| B.保持温度和容器内压强不变,充入1.0 mol SO3 |
| C.降低温度 |
| D.移动活塞压缩气体 |
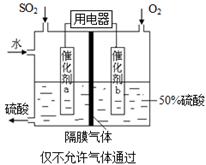
(5)为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为_____。
氮有多种氧化物,其中N2O5是一种新型硝化剂,其性质和制备收到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) 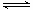 4NO2(g)+O2(g) ;⊿H>0
4NO2(g)+O2(g) ;⊿H>0
①反应达到平衡后,若再通入一定量氩气,则N2O5的转化率将___(填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
③一定温度下,在2L恒容密闭容器中加入2mol N2O5,达到平衡时,气体的压强为原来的
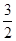 ,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。(2)如图所示装置可用于制备N2O5,则N2O5在电解池的__________区生成,其电极反应式为_________________________________。
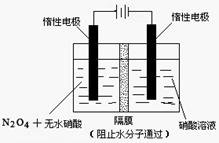
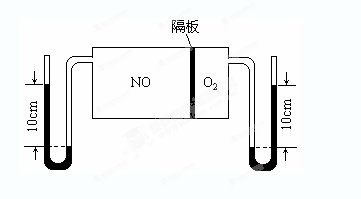
(3)如图:V(NO):V(O2)=3:1。当抽去NO和O2之间的隔板后,NO和O2反应后成NO2,部分NO2聚合成N2O4(N2O4此时为气态)。当体系达到平衡后,U形毛细管两端汞面高度差由反应前10cm变为7.1cm。假设温度不变,且隔板及U形毛细管的体积都忽略不计,此时混合气体的平均相对分子质量为__________。
把大气中的游离态的氮转化为氮的化合物的过程称为固氮。生物固氮和大气固氮(闪电时N2转化为NO)属于自然固氮,这远不能满足人类的需要。工业固氮(合成氨)是目前人工固氮的主要方法。有关大气固氮和工业固氮的平衡常数K值分别如下表一和表二。
表一:N2+ O2  2NO
2NO
| 温度 | 27℃ | 2000℃ |
| K值 | 3.84×10-31 | 0.1 |
表二:N2+ 3H2
 2NH3
2NH3 | 温度 | 25℃ | 350℃ | 400℃ | 450℃ |
| K值 | 5×108 | 1.847 | 0.507 | 0.152 |
A、N2+ O2
 2NO是吸热反应
2NO是吸热反应B、人类大规模模拟大气固氮是没有意义的
C、在常温下,增加工业固氮的容器的压强,K值会发生改变
D、工业固氮是放热反应
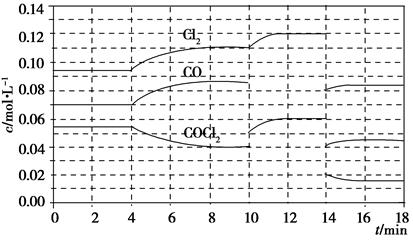
(2)向某密闭容器中加入4 mol NH3、1.2 mol H2和一定量的N2三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知0~t1阶段保持恒温、恒容,且c(N2)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件。

①若t1="15" s,则t0~t1阶段的反应速率为v(H2)=
②N2的起始物质的量为
③反应达到平衡状态,下列说法中能表明已达到平衡状态的是
A、单位时间内生成a molN2,同时生成3a mol H2 B、容器的总压强不再变化
C、混合气体的密度不再变化 D、三个H—H 键断裂的同时有六个H—N键断裂
④t4时刻改变的条件为 ,t5时刻改变的条件为
⑤已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q为正值),试写出该反应的热化学方程式:____________________________________________________________________
KI溶液在酸性条件下能与氧气反应。现有以下实验记录:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度(℃) | 30 | 40 | 50 | 60 | 70 |
| 显色时间(s) | 160 | 80 | 40 | 20 | 10 |
(1)该反应的离子方程式为 。
(2)该实验的目的是 。
(3)实验试剂除了1 mol/L KI溶液、0.1 mol/L H2SO4溶液外,还需要的试剂是 ,实验现象为 。
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是 (填字母)。
A.温度 B.试剂的浓度 C.试剂的用量(体积) D.试剂添加的顺序
(5)由上述实验记录可得出的结论是 。
(6)若要进行酸性对反应速率的影响的探究实验,你会采取的措施是 。
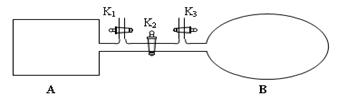
 N2O4已经达到平衡。
N2O4已经达到平衡。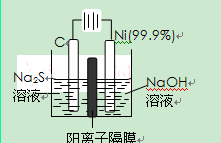
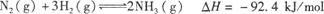 ,据此回答以下问题:
,据此回答以下问题: