题目内容
下列说法正确的是( )
| A、原子的半径越小,其原子序数越大 |
| B、最外层电子数少的原子一定比最外层电子数多的原子易失电子 |
| C、金属性、非金属性强弱从根本上取决于其原子核外电子的排布情况 |
| D、元素的化合价越高,其金属性越强 |
考点:元素周期律和元素周期表的综合应用,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.同主族,原子半径小的原子序数小;
B.最外层电子数少的原子,不一定易失去电子;
C.金属性、非金属性强弱与得失电子能力有关;
D.元素的化合价与金属性无关.
B.最外层电子数少的原子,不一定易失去电子;
C.金属性、非金属性强弱与得失电子能力有关;
D.元素的化合价与金属性无关.
解答:
解:A.同主族,原子半径小的原子序数小,而同周期原子半径小的原子序数大,故A错误;
B.最外层电子数少的原子,不一定易失去电子,如H、He的最外层电子数少,不易失电子,故B错误;
C.金属性、非金属性强弱与得失电子能力有关,则从根本上取决于其原子核外电子的排布情况,故C正确;
D.元素的化合价与金属性无关,金属性与失去电子的能力有关,如Na的金属性大于Al,故D错误;
故选C.
B.最外层电子数少的原子,不一定易失去电子,如H、He的最外层电子数少,不易失电子,故B错误;
C.金属性、非金属性强弱与得失电子能力有关,则从根本上取决于其原子核外电子的排布情况,故C正确;
D.元素的化合价与金属性无关,金属性与失去电子的能力有关,如Na的金属性大于Al,故D错误;
故选C.
点评:本题考查元素周期表和元素周期律的综合应用,为高频考点,把握同主族、同周期元素的性质比较为解答的关键,注意利用实例分析解答,题目难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
鉴别稀硫酸和浓硫酸最简单的方法是( )
| A、加酚酞试液 |
| B、与铜片反应 |
| C、加BaCl2溶液和硝酸 |
| D、用玻璃棒各蘸一点滴在纸上 |
如图是元素周期表的一部分,有关说法不正确的是( )
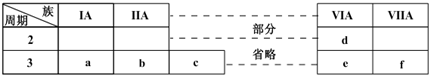

| A、b、d、f四种元素的原子半径:b>f>d |
| B、元素b的单质不能与酸性氧化物发生化学反应 |
| C、元素c的氧化物既能与酸反应,又能与碱反应 |
| D、a、c、e的最高价氧化物对应的水化物之间能够相互反应 |
下列叙述正确的是( )
| A、Fe分别与氯气和稀盐酸反应所得氯化物相同 |
| B、某无色溶液中通入Cl2,溶液变为淡黄色,再加入淀粉溶液,溶液变为蓝色,说明原溶液中存在I- |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、C、N、S三种单质直接与02反应都能生成两种氧化物 |
(双项)下列说法正确的是( )
| A、氢键是一种化学键 |
| B、氢键使物质具有较高的熔、沸点 |
| C、能与水分子形成氢键的物质易溶于水 |
| D、水结成冰体积膨胀与氢键无关 |
化学与社会生活密切相关,下列说法正确的是( )
| A、粘胶纤维、铜氨纤维、涤纶、光导纤维都是有机高分子材料 |
| B、N7H9禽流感病毒并不可怕,人只要喝一定量盐水,就能杀死该病毒 |
| C、有一种新发现的固态碳,称为“纳米泡沫”,外形似海绵,密度小、有磁性,它与金刚石都属于碳的同素异形体 |
| D、分子间作用力比化学键弱得多,它对物质的熔点、沸点有较大影响,但对溶解度无影响 |
下列实验能达到目的是( )
| A、用浓HNO3与Cu反应制备NO2 |
| B、用BaCl2溶液鉴别CO2与SO2 |
| C、用溴水鉴别苯和正已烷 |
| D、将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl |
已知在2L密闭容器内,发生:2NO(g)+O2(g)?2NO2(g),不能说明该反应已达到平衡状态的是( )
| A、容器内颜色保持不变 |
| B、v逆(NO)═2v正(O2) |
| C、单位时间内生成a mol的O2,同时生成2a mol NO2 |
| D、容器内密度保持不变 |