题目内容
1.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA.√(判断对错)分析 每个NO2和CO2分子均含有2个O原子,故二者混合气体中含有O原子数目为分子总数的2倍.
解答 解:每个NO2和CO2分子均含有2个O原子,故分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA,故正确,故答案为:√.
点评 本题考查微粒数目有关计算,比较基础,注意对化学式意义的理解,有利于基础知识的巩固.

练习册系列答案
相关题目
4.下列有关说法正确的是( )
| A. | 蔗糖、淀粉、蛋白质、油脂都是营养物质,都属于高分子化合物,都能发生水解反应 | |
| B. | 人造纤维、合成纤维、碳纤维、光导纤维主要成分都是纤维素 | |
| C. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
5.砷(As)元素与P元素同一主族,下列关于砷(As)元素的叙述不正确的是( )
| A. | 最高价氧化物的化学式为As2O5 | |
| B. | 气态氢化物的稳定性强于磷化氢而弱于硫化氢 | |
| C. | 砷单质在通常状况下为固态 | |
| D. | 砷酸是一种弱酸,酸性比磷酸酸性弱 |
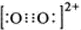 ,1个O22+中含有2个π键.
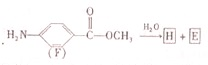
,1个O22+中含有2个π键.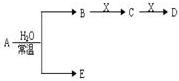 已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去).
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去). .
.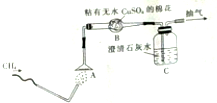 为了验证甲烷的燃烧产物,某同学设计了甲烷的燃烧实验(如图所示):
为了验证甲烷的燃烧产物,某同学设计了甲烷的燃烧实验(如图所示):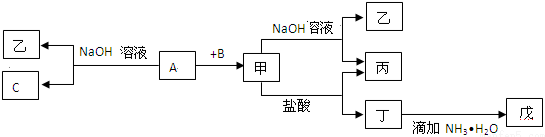
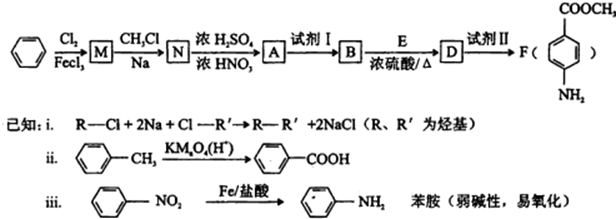
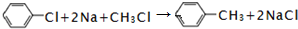 .
.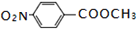 .
.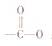 ;
;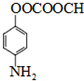 .
.
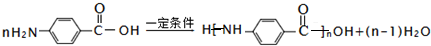 .
.