题目内容
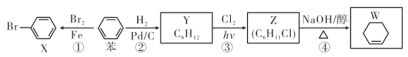
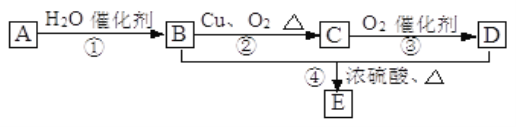
【题目】Ⅰ.如图所示,已知有机物A 的一种同系物的产量,是衡量一个国家石油化工水平的标志,且0.1mol A在足量的氧气中完全燃烧,生成0.3 mol CO2和0.3 mol水。B和D都是有机物,E是具有浓郁香味、不易溶于水的油状液体。
已知:-CHOH最终不能被氧化为—COOH
(1)写出A的结构简式_______。
(2)写出B的结构简式为_______,D中官能团的名称为_______。
(3)写出下列反应的类型:①_______,④_______。
(4)写出下列物质转化的化学方程式: B→C _________ ;B+D→E ______________。
Ⅱ.在实验室可以用如图所示的装置进行B与D的反应,请回答下列问题:

(1)装置中通蒸气的导管要在试管中液面的上方,该溶液的作用是_______。
(2)若要把制得的E分离出来,应采用的实验操作是_______。
Ⅲ. 苹果醋是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果酸是苹果醋的主要成分,其结构简式如图所示,请回答下列问题:
![]()
(1)在一定条件下,苹果酸可能与下列哪些物质发生反应?_______
A.氢氧化钠溶液 B.乙酸 C.碳酸氢钠溶液 D.乙醇
(2)0.1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气_______L。
【答案】CH2=CHCH3 HOCH2CH2CH3 羧基 加成反应 酯化反应(或取代反应) 2CH3CH2CH2OH+O2![]() 2CH3CH2CHO+2H2O CH3CH2COOH+CH3CH2CH2OH
2CH3CH2CHO+2H2O CH3CH2COOH+CH3CH2CH2OH![]() CH3CH2COOCH2CH2CH3+H2O 除去粗产品中多余的酸和醇,降低酯的溶解度有利于酯分离 分液 ABCD 3.36
CH3CH2COOCH2CH2CH3+H2O 除去粗产品中多余的酸和醇,降低酯的溶解度有利于酯分离 分液 ABCD 3.36
【解析】
Ⅰ.A是烯烃,与水发生加成,得到醇,经过连续两次氧化,得到酸,酸和醇反应得到酯;
Ⅱ.醇和酸在浓硫酸的作用下生成酯,酯不溶于水,分离互不相溶的液体用分液;
Ⅲ.1个苹果酸分子中含有2个—COOH,1个—OH,根据官能团的性质推测有机物的性质。
Ⅰ.有机物A的一种同系物的产量,是衡量一个国家石油化工水平的标准,该同系物为乙烯,则A为烯烃。0.1molA在足量的氧气中完全燃烧,生成0.3molCO2和0.3molH2O;则1molA中含有3molC和6molH,则A的分子式为C3H6,为丙烯。丙烯与水发生加成反应,得到B,并最终氧化到丙酸,根据已知-CHOH最终不能被氧化为—COOH,则醇中含有-CH2OH的结构,B为1-丙醇;C为丙醛,D为丙酸,E为丙酸和1-丙醇生成的酯。
(1)A为丙烯,结构简式为CH2=CHCH3;
(2)CH2=CHCH3与水发生加成生成的醇有CH3CH(OH)CH3和CH3CH2CH2OH,B经过连续两次氧化最终得到了丙酸,根据已知,B的结构简式为CH3CH2CH2OH;D为丙酸,官能团的名称为羧基;
(3)反应①为丙烯与水反应生成1—丙醇,为加成反应;反应④为1-丙醇和丙酸生成酯的反应,为酯化反应,也是取代反应;
(4)B生成C为醇的催化氧化,化学方程式为2CH3CH2CH2OH+O2![]() 2CH3CH2CHO+2H2O;B和D生成E,为醇和酸反应生成酯,在酯化反应中酸脱去羧基中的羟基,醇脱去羟基中的氢,化学方程式为CH3CH2COOH+CH3CH2CH2OH
2CH3CH2CHO+2H2O;B和D生成E,为醇和酸反应生成酯,在酯化反应中酸脱去羧基中的羟基,醇脱去羟基中的氢,化学方程式为CH3CH2COOH+CH3CH2CH2OH![]() CH3CH2COOCH2CH2CH3+H2O;
CH3CH2COOCH2CH2CH3+H2O;
Ⅱ.(1)该溶液为饱和碳酸钠溶液,可以中和挥发出来的丙酸,可以溶解挥发出来的1—丙醇,降低酯在水中的溶解度,使之分层效果更好,答案为除去粗产品中多余的酸和醇,降低酯的溶解度有利于酯分离;
(2)酯类不溶于水,所以最终会得到酯层和水层互不相溶的液体,对于互不相溶的液体,分离方法使用分液;
Ⅲ.苹果酸中含有羧基和羟基,按照官能团可以分析苹果醋所具有的性质;(1)苹果醋中含有—COOH,具有酸性,可以与NaOH反应,也可以与碳酸氢钠溶液反应生成CO2;也可以与醇反应生成酯;苹果酸中有羟基可以与羧酸发生酯化反应。ABCD均符合题意;
(3)苹果酸中的羧基和羟基均可以与Na反应,1mol苹果酸可以与Na反应,提供3molH原子生成1.5molH2,在标准状况下的体积为33.6L。则0.1mol苹果酸,生成氢气的体积在标准状况下为3.36L。

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案