题目内容
反应2SO2+O2 2SO3,5s内SO3的浓度增加了0.4 mol/L,则在这段时间内用O2表示的反应速率(mol/L·s)为
2SO3,5s内SO3的浓度增加了0.4 mol/L,则在这段时间内用O2表示的反应速率(mol/L·s)为
 2SO3,5s内SO3的浓度增加了0.4 mol/L,则在这段时间内用O2表示的反应速率(mol/L·s)为
2SO3,5s内SO3的浓度增加了0.4 mol/L,则在这段时间内用O2表示的反应速率(mol/L·s)为| A.0.1 | B.0.08 | C.0.04 | D.0.02 |
C
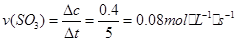 ,从而可知
,从而可知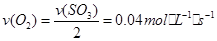 ,故答案为C
,故答案为C
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
题目内容
 2SO3,5s内SO3的浓度增加了0.4 mol/L,则在这段时间内用O2表示的反应速率(mol/L·s)为
2SO3,5s内SO3的浓度增加了0.4 mol/L,则在这段时间内用O2表示的反应速率(mol/L·s)为| A.0.1 | B.0.08 | C.0.04 | D.0.02 |
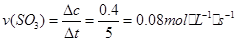 ,从而可知
,从而可知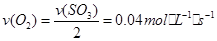 ,故答案为C
,故答案为C
 名校课堂系列答案
名校课堂系列答案