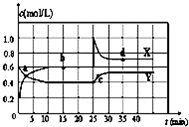
题目内容
对于反应mA(g)+nB(g)=pC(g)+qD(g),根据对应图象填空:
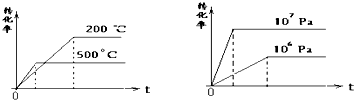
(1)正反应为______反应
(2)m+n______p+q
(3)若图象如图:
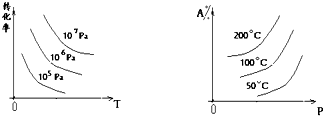
正反应为______反应:m+n______p+q.

(1)正反应为______反应
(2)m+n______p+q
(3)若图象如图:

正反应为______反应:m+n______p+q.
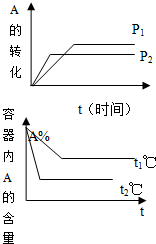
(1)由图可知,升高温度,反应物的转化率降低,说明平衡向逆反应方向移动,则正反应为放热反应,故答案为:放热;
(2)由图可知,增大压强,反应物的转化率增大,说明平衡向正反应方向移动,则正反应为气体体积减小的反应,即m+n>p+q,故答案为:>;
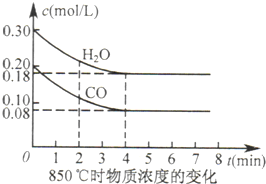
(3)由图可知,温度不变,增大压强,反应物的转化率增大,说明平衡向正反应方向移动,则正反应为气体体积减小的反应,即m+n>p+q;压强不变,升高温度,A的百分含量增大,说明平衡向逆反应方向移动,则正反应为放热反应,故答案为:放热;>.
(2)由图可知,增大压强,反应物的转化率增大,说明平衡向正反应方向移动,则正反应为气体体积减小的反应,即m+n>p+q,故答案为:>;
(3)由图可知,温度不变,增大压强,反应物的转化率增大,说明平衡向正反应方向移动,则正反应为气体体积减小的反应,即m+n>p+q;压强不变,升高温度,A的百分含量增大,说明平衡向逆反应方向移动,则正反应为放热反应,故答案为:放热;>.

练习册系列答案
相关题目