题目内容
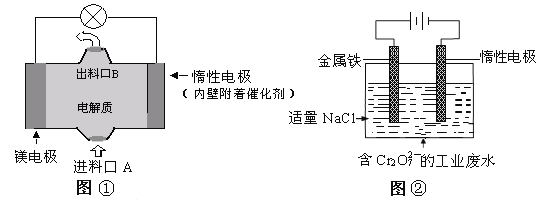
【题目】请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求写出计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是 (填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
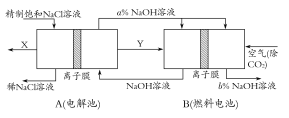
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应,正极: ;负极: ;
③这样设计的主要节(电)能之处在于(写出2处) 、 。
【答案】(1)k=Mr(Cl2)/2Mr(NaOH)=71/80=1∶1.13或0.89
(2)③①②
(3)①Cl2 H2 a%<b%
②O2+4e-+2H2O=4OH- H2-2e-+2OH-=2H2O
③燃料电池可以补充电解池消耗的电能 提高产出碱液的浓度,降低能耗(其他合理答案也可)
【解析】(1)据化学方程式2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑即可计算出k值.
2NaOH+H2↑+Cl2↑即可计算出k值.
(2)把Na2CO3放在BaCl2之后,以除去过量的Ba2+;把盐酸放在NO2CO3之后,以除去过量的CO32-。
(3)判断出二极是解答二池问题的前提:燃料电池中通空气(氧化剂)的一极应为正极,所以:①Y(通入负极,还原剂)必为H2,继而H2产生于电解池的阴极,可推出产生于电解池阳极的X必为Cl2;a% NaOH进入燃料电池,出来后的浓度变化可用二种方法判断:[方法一]从Na+的移动方向来定:Na+向阴极(即正极)移动,所以正极b% NaOH浓度增大,负极流出的NaOH变稀;[方法二]从水、OH-的量变来定:负极H2-2e-+2OH-=2H2O,水增多、OH-减少,变稀;正极O2+4e-+2H2O=4OH-,水减少、OH-增多,所以正极增浓,即a<b。

【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
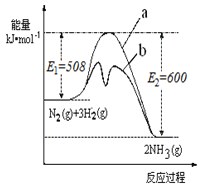
(1)根据如图提供的信息,写出该反应的热化学方程式 ,下图的曲线中 (填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
(2)在恒容容器中,下列描述中能说明上述反应已达
平衡的是 。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 | 1/3 | 1 |
ⅱ | 1/3 | 10 | |
ⅲ | 480 | 10 |