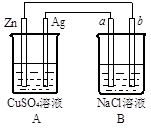题目内容
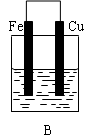
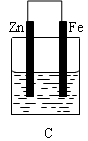
某实验小组用以下几个实验装置探究电化学过程对金属与稀硫酸反应速率的影响, 烧杯中都盛有稀H2SO4。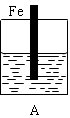
试回答:
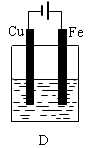
(1)B装置中Cu电极上的电极反应式为 ,D装置中Fe电极上的电极反应式为 。
(2)D装置中的实验现象有 ,若用电流表测量反应时通过导线的电子流量为0.2mol,则Fe电极的质量变化为 。
(3)B、C两个装置中Fe片被腐蚀的速率更快的是 (填B或C)。
(1) 2H++2e-=H2 ↑,Fe-2e-=Fe2+。
(2)Cu电极上有气泡,Fe电极逐渐溶解,溶液逐渐变为浅绿色,减小5.6g。 (3)B
解析试题分析:(1)在B装置中由于活动性Fe>Cu,所以Cu电极为原电池的正极,在正极上的电极反应式为2H++2e-=H2↑,D装置为电解池。由于在D装置中Fe电极与直流电源的正极相连接,所以为阳极。在Fe电极上的发生氧化反应,电极反应式为Fe-2e-=Fe2+。(2)在D装置中可看到的实验现象有Fe电极逐渐溶解消耗,在Cu电极上不断有气泡产生。同时溶液逐渐由无色变为浅绿色。若用电流表测量反应时通过导线的电子流量为0.2mol,因为Fe是+2价的金属,则Fe电极消耗的物质的量为0.1mol,由于Fed的摩尔质量为56g/mol,所以其质量变化为减少5.6g,(3)由于金属活动性Zn>Fe>Cu.所以在B装置中Fe为原电池的负极,被氧化而腐蚀;在C装置中Fe片作原电池的正极,首先被腐蚀的是活动性强的Zn,Fe被保护起来。因此在B、C两个装置中被腐蚀的速率更快的是B。
考点:考查电化学过程对金属与稀硫酸反应速率的影响及金属的腐蚀与保护的知识。

用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是( )
| A.稀NaOH溶液 | B.HCl溶液 | C.NaCl溶液 | D.酸性AgNO3溶液 |
(6分)ZnMnO2干电池应用广泛,其电解质溶液是ZnCl2NH4Cl混合溶液。
(1)该电池的负极材料是________。电池工作时,电子流向________(填“正极”或 负 )。
(2)若ZnCl2NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是____________。
欲除去Cu2+,最好选用下列试剂中的________(填代号)。
| A.NaOH | B.Zn | C.Fe | D.NH3·H2O |
某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64)。
按照实验步骤依次回答下列问题:
(1)导线中电子流向为__________________(用a、b表示)。
(2)写出装置中锌电极上的电极反应式:____________________________________;
(3)若装置中铜电极的质量增加0.64 g,则导线中转移的电子数目为________;(不许用“NA”表示)
(4)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是________。
| A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动 |
| B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动 |
| C.盐桥中的K+、Cl-都向左侧烧杯移动 |
| D.盐桥中的K+、Cl-几乎都不移动 |