题目内容
【题目】下列关于氯水的说法正确的是( )
A. 新制氯水含有Cl2、HCl、HClO、H2O分子
B. 紫色石蕊试剂滴入新制氯水中,溶液先变红后变无色
C. 氯水和液氯都能使干燥的有色布条褪色
D. 新制氯水的pH值要比久置氯水的pH值小
【答案】B
【解析】
A.氯气与水发生Cl2+H2O![]() HClO+HCl,溶液中含有Cl2、HClO、H2O分子,含有OH-、H+、ClO-、Cl-等离子,新制氯水中无HCl分子,故A错误;
HClO+HCl,溶液中含有Cl2、HClO、H2O分子,含有OH-、H+、ClO-、Cl-等离子,新制氯水中无HCl分子,故A错误;
B.氯水中含有盐酸和次氯酸,溶液呈酸性,次氯酸有漂白性,所以紫色石蕊试剂滴入新制氯水中,溶液先变红后变无色,故B正确;
C.氯气没有漂白性,起漂白作用的是次氯酸,液氯无水,因此液氯不能使干燥的有色布条褪色,故C错误;
D.久置氯水中的次氯酸见光易分解,生成HCl和O2,酸性增强,所以新制氯水的pH值要比久置氯水的pH值大,故D错误;
故答案选B。

【题目】CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
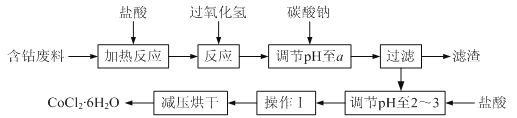
已知:①CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,易失去结晶水变成有毒的无水氯化钴。(乙醚:无色液体,沸点34.5℃,在水中的溶解度小)
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)钴的性质与铁相似,能与盐酸和硝酸反应,写出钴与盐酸反应的化学方程式:________________________________。
(2)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点:
①为__________________________,防止大气污染;
②防止产品中混有硝酸盐。
(3) 加入碳酸钠调节pH至a,a的范围应是5.2~_________。
(4) 操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和_________。
(5)根据表中数据,判断Ksp[Fe(OH)3] ________Ksp[Co(OH)2] (填“<”、“=”或“>”) 。在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是:将产品溶于乙醚过滤后,再蒸馏。

